Anbefalinger
- Vi anbefaler at gravide med moderat og alvorlig hjerte/karsykdom følges opp av tverrfaglig team bestående av kardiolog, gynekolog, anestesiolog samt øvrige relevante spesialiteter1,2 (IV)
- Vi foreslår at det utarbeides en tverrfaglig fødselsplan (IV)
- Vi anbefaler at alvorlig hjertesyke gravide i mWHO klasse IV skal henvises til Nasjonal behandlingstjeneste for hjertesyke gravide og behandles og føde ved Oslo Universitetssykehus-Rikshospitalet 3
- Vi foreslår at kvinner med moderat og alvorlig hjerte/karsykdom bør tilbys prekonsepsjonell veiledning, inkludert genetisk veiledning der det er indisert1 (IV)
- Vi foreslår at hjertesyke kvinner som behandles med betablokker følges med fostertilvekst hver 4-6.uke (III)
- Vi foreslår vaginal forløsning for majoriteten av hjertesyke kvinner, med visse unntak4 (III)
- Vi foreslår at det utføres ekkokardiografi ved nyoppståtte kardiopulmonale symptomer i graviditet/barseltid (IV)
- Vi foreslår ikke endokardittprofylakse under fødsel, med visse unntak (III)
Søkestrategi
Pyramidesøk Mc Master plus, Cochrane Database, Pubmed, UptoDate, The Task Force for the Managament of Cardiovascular Diseases during Pregnancy of the European Society of Cardiology; European Society of Cardiology, Royal College of Obstetrics and Gynaecology. Vitenskapelig dokumentasjon er mangelfull og det er ingen store randomiserte kontrollerte eller prospektive studier. Anbefalingene bygger i stor grad på retrospektive observasjonsstudier og case-series som oppsummert i internasjonale retningslinjer (ESC2,5 og RCOG6).
Søkeord for app-versjonen
Hjertesykdom, hjerte-/karsykdom, GUCH, aortasykdom, mekanisk hjerteklaff.
Linker: Trombose, antikoagulasjon og svangerskap; Smertelindring.
Definisjon
Medfødt eller ervervet hjertesykdom samt sykdommer som affiserer aorta i graviditet/fødsel.
Epidemiologi
Hjertesyke gravide deles inn i 5 grupper etter hvilken type hjertesykdom som foreligger:
- Medfødte hjertefeil
- Kardiomyopatier
- Aortopatier
- Ervervet hjertesykdom (feks. revmatisk klaffefeil; ischemisk klaffesykdom)
- Arytmier
Hjertesykdom (både medfødt og ervervet) kompliserer 1–4 % av alle svangerskap i høyinntektsland. Andelen gravide med koronar hjertesykdom er økende, noe man tror skyldes eldre førstegangsfødende og økt forekomst av risikofaktorer som diabetes, hypertensjon og overvekt. Ikke-diagnostisert hjertesykdom som avdekkes i svangerskapet, ser vi hovedsakelig blant innvandrerkvinner og asylsøkere. Revmatisk klaffesykdom dominerer blant innvandrere fra lav- og middelinntektsland.
Det bør være lav terskel for å henvise kvinner til ultralyd av hjertet ved symptomer som dyspnoe, ødemer og takykardi7, 8. Dette er viktig for å kunne oppdage ikke erkjent hjertesykdom som debuterer med symptomer i svangerskapet.
Risikostratifisering ved modifisert WHO (mWHO)
Gravide kvinner med hjertesykdom skal risikovurderes utfra hvilken hjertefeil mor har9. Risikovurderingen bestemmer hvor tett kvinnen skal følges opp, hvor hun skal følges opp, og om hun i det hele tatt bør bli gravid.Kvinner inndeles i 5 kategorier basert på modifisert WHO klassifisering10 (Tabell 1).
Risikoen hos disse pasientene må vurderes fortløpende gjennom svangerskapet, idet forverring under graviditeten kan medføre at hun blir klassifisert i en høyere risikogruppe enn ved starten av svangerskapet. Dette krever tett tverrfaglig samarbeid mellom spesialister og profesjoner samt god dialog mellom behandlende sykehus hvor kvinnen skal følges, behandles og forløses.
Tabell 1 Modifisert World Health Organization10 (mWHO) klassifisering av hjertesykdom i svangerskap
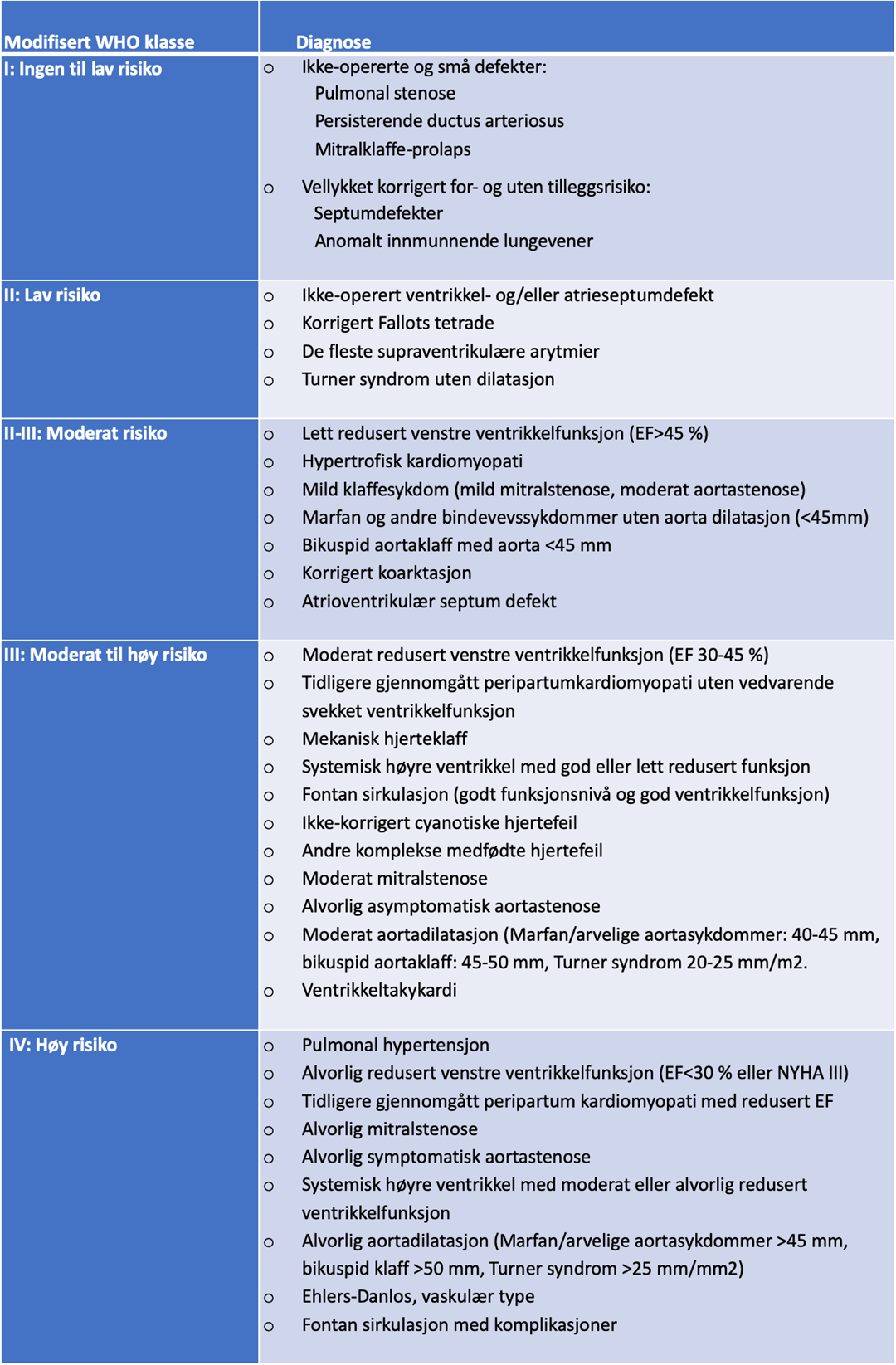
EF: ejeksjonsfraksjon. NYHA= New York Heart Association. WHO= World Health Organization.
Oppfølging/Behandling
Før svangerskap
Kvinner med medfødt hjertesykdom bør fra tidlig i tenårene få informasjon om hvordan et eventuelt svangerskap i fremtiden vil påvirke helsen deres, samt råd om riktig prevensjon5. Tverrfaglig prekonsepsjonell veiledning bør tilbys alle hjertesyke kvinner1. Kvinner med moderat eller høy risiko for kardiovaskulær hendelse under svangerskap bør henvises til regionsykehus som har spesiell kompetanse på dette området.
Prekonsepsjonell veiledning
- Risikovurdering for mor og foster
- Medikamentgjennomgang med tanke på fosterskadelige medikamenter
- Ekkokardiografi og funksjonstesting (evt. MR)
- Generelle råd om røyking, mosjon og livsstil
Ved diagnostisering/oppfølging av hjertesykdom hos mor foretrekkes ekkokardiografi av hjertet, funksjonstester og MR (uten kontrast). Dersom prosedyrer må gjennomføres, er det lavest risiko for abort/fosterkomplikasjoner i andre og tredje trimester.
Fertilitetsutredning og -behandling
Ved ART, bør den økte risiko for trombose og hyperstimulerings syndrom tas i betraktning i forhold til valg av hormonell terapi2. Single-embryo transfer anbefales. Blant kvinner i klasse mWHO III eller som er terapeutisk antikoagulert bør fertilitetsbehandling skje i nært samarbeid med kardiolog. Ved visse hjertetilstander (Fontan, pulmonal hypertensjon) kan hysteroskopi og laparoskopi medføre komplikasjoner og bør utføres ved sentre med nødvendig kompetanse. Fertilitetsbehandling er kontraindisert i mWHO klasse IV.
Svangerskap
Alle kvinner med kjent hjerte- eller aortasykdom bør ved erkjent svangerskap vurderes for henvisning til spesialisthelsetjenesten i første trimester.
Risiko for komplikasjoner i svangerskap avhenger av den underliggende hjertediagnosen, ventrikkel- og klaffefunksjon, mWHO klasse, tilstedeværelse av cyanose, pulmonal hypertensjon og andre faktorer.
Blant gravide med hjertesykdom foreligger det økt risiko for preeklampsi, preterm fødsel og postpartum blødning11. Føtale komplikasjoner forekommer i 18-30 % av svangerskap, der den viktigste komplikasjonen er prematuritet (hovedsakelig iatrogen) samt tilveksthemning11. Neonatal mortalitet forekommer i 1-4 % av svangerskap, men med store variasjoner avhengig av mors hjertetilstand. Ved maternell medfødt hjertesykdom foreligger det en økt risiko for hjertesykdom hos foster (2-20 %) avhengig av type hjertefeil.
- Gravide i mWHO klasse II og oppover skal følges av et tverrfaglig team ved sykehus som har den nødvendige kompetansen2,6.
- Hjertesyke kvinner i mWHO klasse IV frarådes svangerskap. Dersom graviditet oppstår, bør avbrytelse av svangerskapet være diskutert med kvinnen. Gravide i mWHO klasse IV skal kontrolleres og føde ved Oslo Universitetssykehus Rikshospitalet (OUS-RH)3.
Abort
Ved svangerskapsavbrudd eller inkomplett spontanabort bør behandlingsmetode individualiseres. Medisinsk abort med misoprostol kan etter vanlige retningslinjer vurderes uavhengig av svangerskapslengde. Pga risiko for blødning og abort etter inntak av mifepristone bør kvinner i mWHO III-IV innlegges ved inntak av mifepristone ved senter med nødvendig anestesiologisk kompetanse.
Tverrfaglig team
Kvinner i moderat til høy risikoklasse (mWHO II-III, III og IV) bør tilbys oppfølging av et spesialisert tverrfaglig team. Det tverrfaglige teamet bør minimum bestå av gynekolog, kardiolog med GUCH-kompetanse og anestesilege. I tillegg anbefales det tett samarbeid med hematolog, thoraxkirurg og nyfødtlege.
Fosterdiagnostikk
- Kvinner med medfødt hjertefeil kan tilbys utvidet ultralyd/ekkokardiografi ved fostermedisinsk avdeling i svangerskapsuke 18-21
- Fosterdiagnostisk ultralyd i første trimester kan tilbys kvinner med alvorlig hjertesykdom (mWHO klasse III-IV) idet svangerskap i denne gruppen kan utgjøre en betydelig fysisk belastning/risiko
Oppfølging
- Svangerskapskontrollene bør skje tverrfaglig og bør individualiseres
- Ved erkjent svangerskap skal ACE-hemmer seponeres
- Vurder acetylsalisylsyre (Albyl-E© 75 mg) fra uke 12-37 for kvinner med høy til moderat risiko for preeklampsi
- Kvinner med moderat til alvorlig hjertesykdom (mWHO II-III, III og IV) bør følges med regelmessige, individualiserte og tverrfaglige kontroller inklusive fostertilvekst fra svangerskapsuke 23-24
- Ved bruk av betablokker foreslår vi tilvekstkontroller hver 3-4 uke i 3.trimester
- Ved tegn på intrauterin vekstrestriksjon følges fosteret etter ordinære retningslinjer (se kapittel Intrauterin vekstrestriksjon).
- Kontroller bør kartlegge kardiopulmonale symptomer som dyspnoe, nærsyncope, hjertebank, arrytmi, ødemer
- Måling av maternelt BT, puls, auskultasjon cor/pulm, perifere ødemer, urinfunn
Kardiologisk undersøkelse, evt. ultralyd av hjertet, EKG - Ev. funksjonstesting, for eksempel trappetest
Medikasjon
Antiarrytmika
Betablokkere er effektive antiarrytmika og er generelt trygt å bruke i svangerskapet, tilvekstkontroller skal da utføres. Ved behov for betablokkade er beta1-selektive blokkere foretrukket (for eksempel metoprolol) grunnet økt risiko for tilveksthemning ved ikke-selektive blokkere. Ved OUS-RH anbefales screening for neonatal hypoglykemi i løpet av første levedøgn dersom mor behandles med betablokker.
Antihypertensiva
Behandling av hypertensjon blant hjertesyke gravide følger de samme prinsippene som for ikke-hjertesyke gravide.
Antikoagulasjon
Det er store variasjoner i antikoagulasjonsbehandling av gravide rundt om i verden2. Ved mekanisk aorta- eller mitralklaff og behov for antikoagulasjonsbehandling kan pasienter behandles med lavmolekylært heparin (LMWH) gjennom hele svangerskapet eller de kan behandles med oral antikoagulasjon (OAC) (Warfarin) fra 12 svangerskapsuke. Risiko for ventiltrombose i svangerskap er betydelig redusert ved DOAK-behandling sammenliknet med ufraksjonert heparin (UHF)2. På den annen side passer OAC placenta og har fosterskadelige effekter med økt risiko for misdannelser og føtal hjerneblødning (dose > 5 mg per dag). Det er p.t. ingen konsensus hvorvidt man skal behandle gravide med LMWH i hele svangerskapet eller med DOAK i deler av svangerskapet (uke 12–36).
LMWH kan følges med anti-Xa målinger med terapeutisk nivå 0,8–1,2 U/ml, men dette er ikke et absolutt krav. Vurder maksimal dose i forhold til pasientens vekt (for dalteparin vil doseringen være 120 IE / kg x 2). Se for øvrig kapittelet Trombose antikoagulasjon og svangerskap.
Fødsel
Fødselsplan
Alle hjertesyke gravide bør i god tid før fødselen få utarbeidet en individuell journalført fødselsplan ved starten av 3.trimester1. Fødselsplanen bør inneholde forløsningsmetode (vaginal/keisersnitt), ønsket sterilisering hvis keisersnitt, tid for forløsning (spontan/indusert), smertelindring, nødvendig monitorering, endokardittprofylakse, terskel for operativ forløsning, grad av overvåkning i barsel, informasjon om spesielle risikofaktorer og evnt. etterkontroll. Kvinnen bør være informert om planen.
Fødested
Hjertesyke gravide med moderat og høy risiko svangerskap (mWHO II-III, III) bør føde ved regionsykehus som har nødvendig tverrfaglig team med kompetanse og erfaring med hjertesykdom hos gravide1. Dersom det ikke foreligger nødvendig tverrfaglig kompetanse kan kvinnen henvises til Nasjonal behandlingstjeneste for hjertesyke gravide ved OUS-RH3. Kvinner i mWHO klasse IV skal føde ved OUS-RH.
Timing av fødsel
Induksjon av fødsel kan vurderes på individuell basis ved termin for kvinner med moderat til alvorlig hjertesykdom2. Timing vil avhenge av kardiell diagnose og status, obstetrisk evaluering inklusive paritet og cervixstatus, føtal vekt og lungemodning.
Valg av metoder for induksjon av fødsel er stort sett som hos friske kvinner. Hos kvinner med lang QT-tid syndrom (LQTS) skal det utvises forsiktighet med oxytocin.
Forløsningsmetode
De aller fleste hjertesyke gravide kan føde vaginalt, men for en liten subgruppe risikopasienter må det gjøres en individuell risikovurdering2,4. I tillegg til hjertesykdom bør andre tilleggsfaktorer (overvekt, vanskelig luftvei, hypertensjon) tas med i vurdering av forløsningsmetode. Akutt keisersnitt, og særlig grad 1 keisersnitt kan medføre økt risiko for mor dersom det ikke er tid til regionalanestesi eller adekvat hemodynamisk monitorering.
Vaginal fødsel er assosiert med store hemodynamiske forandringer. God smertelindring (epidural) er viktig. Epiduralanalgesi har god effekt på smerter under fødselen, men reduserer ikke de relativt store fluktasjonene i puls, blodtrykk, perifer motstand og hjerteminuttvolum.
Elektivt keisersnitt anbefales2 til gravide med:
- peroral antikoagulasjon (Warfarin)
- Marfan syndrom med aortadiameter >45 mm (vurderes også mellom 40-45 mm)
- aortadisseksjon (akutt/kronisk eller tidligere disseksjon)
- alvorlig hjertesvikt (EF < 30 %, NYHA klasse III-IV)
På individuelt grunnlag bør elektivt keisersnitt vurderes ved:
- alvorlig aortastenose/mitral stenose/hypertrofisk obstruktiv kardiomyopati
- alvorlig pulmonal hypertensjon (inklusive Eisenmenger syndrom) og cyanotisk hjertesykdom
- symptomgivende ischemisk hjertesykdom
Overvåkning/tiltak under fødsel
Hemodynamisk monitorering under fødsel er viktig for å detektere tidlige tegn på maternell
dekompensasjon, slik at fødsel kan framskyndes.
- Monitorering av maternell BT, puls
- Telemetri
- Intravenøs tilgang (1-2 venfloner og Ringer infusjonsvæske klar til bruk)
- Leie - unngå aortocaval kompresjon
- Kontinuerlig CTG/STAN anbefales
- Evt. arteriekran til kvinner med høyrisiko hjertesykdom
- Adekvat smertelindring med epidural, evnt. i.v remifentanilinfusjon der regionalanalgesi er kontraindisert
- Sikre god descens av presenterende del for å unngå langvarig trykkefase
Tang/vakuum vurderes ved behov for å forkorte utdrivningsfasen - Aktiv forløsning av placenta samt gi ordinær oxytocinprofylakse mot postpartumblødning12. Oxytocin og/eller misoprostol i 3.stadium har liten hemodynamisk betydning. Obs: ved LQTS anbefales forsiktig titrering av oxytocin.
Ergometrin og carboprost bør unngås pga alvorlige bivirkninger.
Terapeutisk antikoagulasjon rundt fødsel (ikke ved mekanisk klaff):
Ved tvil, konferer hematolog for individualisert plan.
Planlagt keisersnitt
Lavdose/høydose LMWH: seponeres 24 timer før operasjon. Gjenopptas 6 timer postoperativt, evnt. i lavere vektjusterte doser avhengig av klinisk situasjon. Dersom forløsning framskyndes kan anti-Xa aktivitet veilede timing av prosedyren. For høyrisiko kvinner kan alternativt ufraksjonert heparin infusjon startes 6 timer etter inngrepet.
Planlagt vaginal fødsel
Lavdose/høydose LMWH: seponeres 24 timer før forventet fødsel/induksjon. Gjenopptas 6 timer etter fødsel. Gi evnt. tilleggsdoser dersom fødsel drøyer.
Akutt forløsning
Økt risiko for peripartum blødning. Vurder antidot: protamin (LMWH), plasma, vitamin K (Warfarin). Kontakt hematolog.
Dersom kvinnen behandles med perorale antikoagulantia (DOAK eller Warfarin):
Keisersnitt minsker risiko for føtal intrakraniell blødning. Fosteret kan være antikoagulert opp til 10 dager etter seponering av maternell DOAK og kan trenge fersk frossen plasma/vitamin K
Anestesi til hjertesyke
Ved anestesi til lavrisiko pasienter følges anbefalinger for spinalanestesi til friske gravide ved sectio. (Se kapittel Smertelindring). Spinalanestesi gir en uttalt vasodilatasjon og en kompensatorisk økning i puls og hjerteminuttvolum13. Denne hemodynamiske effekten kan og skal motvirkes med i.v fenylefrin. Basert på lang erfaring med regionalanestesi til hjertesyke gravide, mener vi at gravide med god venstre ventrikkelfunksjon er hemodynamisk stabile under spinalanestesi ved bruk av profylaktisk i.v fenylefrin for å unngå vasodilatasjon og tachykardi14. Anestesi til gravide med redusert venstre ventrikkelfunksjon bør gis titrert med spinalkateter. For kvinner med moderat og høy risiko i svangerskapet er regionalanestesi anbefalt, bortsett fra ved kontraindikasjoner (blødningsforstyrrelser, antikoagulasjon)15. Hos kvinner med alvorlig hjertesvikt, f.eks. grunnet peripartumkardiomyopati (PPCM) eller dilatert kardiomyopati (DCM) kan det være aktuelt å legge inn aorta-ballongpumpe (IABP) før sectio.
Leie/Unngå aortocaval kompresjon
- Viktig å tippe pasienten godt over i venstre sideleie, og heve overkroppen
- Rask vasking og dekking av operasjonsfelt
Monitorering
- Standard: EKG, SaO2
- Arteriekran for kontinuerlig hemodynamisk monitorering
- CO-monitorering er nyttig perioperativt hos høyrisikopasienter (alvorlig hjertesvikt, PHT, MS, AS, HOCM)
Titrert anestesi
- Spinalanestesi til gravide med god venstre ventrikkelfunksjon
- Kontinuerlig spinal anbefales til gravide kvinner med dårlig venstre ventrikkelfunksjon
Fenylefrin-infusjon og titrerte boluser for å unngå tachykardi
- Pasienter med venstresidige obstruksjoner (AS, MS, HOCM) krever ofte store doser vasopressor for å motvirke fall i perifer motstand og unngå tachykardi
Titrert oxytocin
- Oxytocin gis sakte i titrerte doser (0,1 IE) til effekt
- Kan kombineres med små boluser fenylefrin (30µg) for å motvirke tachykardi og hypotensjon
- Ergometrin og Carboprost bør unngås pga alvorlige bivirkninger
Ved narkose til hjertesyke gravide bør man gi en titrert anestesi med opioider og reduserte doser Pentothal (evt. Ketamine) for å redusere hemodynamisk instabilitet.
Endokardittprofylakse
Endokarditt i svangerskap er sjelden med en insidens på 1 per 100.000 svangerskap. Blant gravide med medfødt hjertesykdom eller klaffefeil er insidensen 0,5 %. Pasienter med høyest risiko er de med kunstig klaff eller tidligere gjennomgått endokarditt. Endokardittprofylakse anbefales ikke ved vaginal fødsel eller keisersnitt ifølge europeiske guidelines16. Ved OUS-RH gir vi fremdeles endokardittprofylakse ved:
- Tidligere gjennomgått endokarditt
- Innsatte klaffeproteser eller rørgraft i større kar
- Hjertetransplanterte med klaffefeil
- Medfødte hjertefeil: komplekse ukorrigerte cyanotiske medfødte hjertefeil, kirurgisk konstruerte pulmonale shunter eller conduit, komplett reparerte medfødte defekter første 6 mnd etter operasjon eller kateterbasert intervensjon, korrigerte medfødte hjertefeil med restdefekter nær reparasjonstedet.
Ved OUS-RH gis endokardittprofylakse med engangsdose amoksicillin 2 g iv 1 time før sectio eller ved start av fødselen. Ved penicillinallergi gir vi clindamycin 600 mg iv.
Barseltid
De første dagene postpartum skjer det store væskeskift som kan medføre forverring i mors tilstand (dyspnoe, lungeødem, arytmier etc), og man bør ha lav terskel for å kontakte kardiolog og vurdere behov for ultralyd av hjertet.
- Hemodynamisk monitorering bør fortsette i 24-48 timer etter fødsel
Ved telemetriovervåkning kan denne kontinueres 24-48 timer etter fødsel - Amming oppfordres med mindre kvinnen har peripartum kardiomyopati (PPCM) eller starter med medikasjon som er kontraindisert ved amming
- Vurdering av medikamenter før hjemreise bør gjøres av kardiolog
- Tromboseprofylakse etter retningslinjer
Prevensjon
Prevensjon som kun inneholder hormonet gestagen anbefales og kan anvendes av alle kvinner som har medfødt hjertefeil eller senere oppstått hjertesykdom10. Kvinner med alvorlig hjertesykdom bør ha sikrest mulig prevensjon som hormonspiral eller implantat (LARC). Gestagen kan redusere effekten av Warfarin. Kontroller INR og vurder om Warfarindosen skal økes.
Bosentan kan redusere effekten av gestagen17. Vurder om gestagendosen skal økes (feks. implantat + «minipille»), eventuelt tilleggsprevensjon i form av kondom.
Østrogenbasert prevensjon anbefales ikke til kvinner som ammer. Hvis kvinnen ikke ammer, frarådes allikevel prevensjon som inneholder østrogen ved følgende tilstander10:
- Mekanisk hjerteklaff
- Dilatert kardiomyopati
- Fontan sirkuasjon og cyanotisk hjertesykdom
- Pulmonal hypertensjon
- Reversible venstre til høyre shunting (feks. ikke-operert ASD)
- Atrieflimmer/-flutter
- Hjertesvikt, redusert venstre ventrikkelfunksjon
- Angina, tidligere hjerteinfarkt
- Tidligere dyp venetrombose
- Hypertensjon
Gestagenbasert nødprevensjon («angrepille») kan tas av alle kvinner med hjertesykdom.
Spiralinnsetting kan utløse vasovagal reaksjon. I risikoklasse mWHO III og IV bør spiral innsettes på sykehus med nødvendig anestesiologisk kompetanse.
Behov og mulighet for sterilisering bør diskuteres med kvinnen som ledd i en fødeplan dersom keisersnitt blir foretatt.
Svangerskap og ulike typer hjertefeil
Medfødt hjertefeil
De fleste kvinner med medfødt hjertefeil tåler å gjennomgå svangerskap. Risikoen for kardiovaskulær hendelse under svangerskapet avhenger av type medfødt hjertefeil og kompleksiteten i denne, særlig når det gjelder ventrikkel- og klaffefunksjon, NYHA-klasse og forekomst av cyanose.
Alle bør vurderes av kardiolog og gynekolog i slutten av første trimester. Kvinner med moderat til høy risiko bør henvises til senter for pasienter med medfødt hjertesykdom (GUCH-senter). Cyanose er en risikofaktor for fosteret og sannsynligheten for levende født barn er < 12 % dersom O2-metningen hos mor er < 85 %. Kvinner med Fontan sirkulasjon kan ha vellykkede svangerskap, med moderat til høy risiko, avhengig av NYHA-klasse og ventrikkelfunksjon før svangerskap.
Lite kunnskap foreligger om hvordan svangerskapene påvirker forverring av medfødt hjertesykdom på sikt.
Pulmonal hypertensjon
Svangerskap frarådes hos pasienter med pulmonal hypertensjon (PHT) og Eisenmenger-syndrom på grunn av betydelig økt risiko for maternell død eller alvorlig hendelse under svangerskapet (30-50 %)18. De store hemodynamiske endringene under svangerskapet gir økt risiko for hjertesvikt og kardial dekompensering, hovedsakelig i forbindelse med fødselen og tiden postpartum.
Dersom en kvinne velger å gjennomgå svangerskap til tross for den økte risikoen, er det svært viktig med tett oppfølging på et senter med tverrfaglig kompetanse innen feltet. Postpartum er nøye monitorering av væskebalanse essensielt, med sikring av en betydelig negativ væskebalanse i løpet av de første 72 timene.
Aortapatologi
Svangerskap utgjør en høy risiko for pasienter med aortapatologi. De hemodynamiske og hormonelle forandringene under svangerskapet påvirker karveggen og gjør denne skjør.
Aortadisseksjon oppstår oftest i siste trimester (50 %) eller tidlig postpartum (33 %). Aortadisseksjon bør overveies som mulig diagnose hos alle med brystsmerter i svangerskapet.
Kvinner som har Marfans syndrom og en aortadiameter > 45 mm, bør frarådes svangerskap (mWHO gr. IV). Dersom økende dilatasjon tilkommer under svangerskapet, må kirurgi vurderes.
Ca. 50 % av kvinner med bicuspid aortaklaff og aortastenose har dilatasjon av aorta ascendens. Disseksjon kan forekomme hos disse under svangerskapet, men sjeldnere enn ved Marfan.
Kvinner med aortapatologi bør følges med hyppige ekkokardiografikontroller i svangerskapet, minimum én ekkokontroll i hvert trimester. Forløsning med sectio bør overveies ved aortadiameter >45 mm.
Klaffefeil
Klaffeinsuffisiens tolereres bedre enn klaffestenose under svangerskap. Behandling før svangerskapet er kun indisert når en stor klaffeinsuffisiens ledsages av hjertesvikt, betydelig ventrikkeldilatasjon eller -dysfunksjon. Det er viktig å være oppmerksom på økende dyspné under svangerskapet.
Kvinner med moderat til alvorlig mitralstenose tolererer dårlig svangerskap. De bør optimalt sett behandles før en eventuell graviditet. For antikoagulasjonsbehandling av mekanisk klaff, se over.
Koronarsykdom
Ved brystsmerter eller andre symptomer på koronarsykdom bør utredning med EKG og blodprøver foretas også av unge gravide (infarktstatus; CKMB og troponin). I den akutte fasen skal gravide utredes og behandles som andre pasienter med koronarsykdom.
Hos kvinner med koronarsykdom eller gjennomgått hjerteinfarkt uten restangina og med god ventrikkelfunksjon (EF > 40 %) kan svangerskap overveies etter prekonsepsjonell vurdering hos kardiolog.
Kardiomyopatier
Hypertrofisk kardiomyopati (HCM/HOCM):
Hypertrofisk kardiomyopati med obstruksjon (HOCM) er høyrisikosvangerskap. Asymptomatiske pasienter uten obstruksjon (HCM) tolererer svangerskap godt. Atrieflimmer tolereres imidlertid dårlig hos disse pasientene, og rytmekontroll til sinusrytme er nødvendig.
Dilatert kardiomyopati (DCM):
Kvinner med dilatert kardiomyopati har økt risiko for forverring og økende dilatasjon under svangerskapet og perioden postpartum. Symptomer er hjertebank, økende dyspné og tegn på hjertesvikt.
Peripartumkardiomyopati (PPCM):
PPCM defineres som hjertesvikt med redusert venstre ventrikkelfunksjon, det vil si EF < 45 % siste måneder av svangerskap, eller i løpet av de 5 første månedene postpartum. Forekomsten er 1 per 3000–15 000 svangerskap. Mortaliteten er opptil 20 %. Det foreligger økt risiko for utvikling av PPCM hos gravide med hypertensjon, preeklampsi og flerlingesvangerskap. Behandling med bromokriptin i akuttfasen har gitt svært lovende resultater og bør vurderes19.
Hjertesvikt
Begynnende hjertesvikt er vanskelig å diagnostisere i svangerskap, da symptomene på begynnende hjertesvikt ofte er de samme som noen kvinner får ved normale svangerskap; dyspné, lett takykardi og hevelse i underekstremitetene. ProBNP (pro-B-natriuretisk peptid) er en markør for hjertesvikt som kan være nyttig for å følge utviklingen av hjertesvikt. Selv om proBNP kan øke litt i normale svangerskapet, vil man se høyere verdier ved utvikling av hjertesvikt. Behandlingen av hjertesvikt hos gravide og i perioden postpartum er som ved konvensjonell sviktbehandling: betablokker, ACE-hemmer (skal kun brukes postpartum) og diuretika.
Arytmier
Under normale svangerskap øker hjertefrekvensen normalt 10–15 slag/min. Erfaring viser at arytmier kan forverres eller oppstå for første gang i et svangerskap. Mest sannsynlig skyldes dette de hormonelle påvirkningene og de store hemodynamiske forandringene som skjer under svangerskapet.
Betablokker, hovedsakelig metoprolol, er førstevalg når det gjelder antiarytmika.
Har man imidlertid hemodynamisk ustabile pasienter med takykardi, bør man overveie elektrokonvertering, som er trygt å utføre i svangerskapet. AV nodal re-entry takykardi eller AV re-entry takykardi kan stoppes med vagusstimulering, eller med intravenøs adenosin som er trygt å gi under graviditet. Det er i dag flere kvinner i fertil alder som har ICD. ICD er ingen kontraindikasjon mot svangerskap.
Hjertetransplanterte
Hjertetransplanterte gravide bør følges opp og behandles av tverrfaglig team ved regionsykehus med transplantasjonssenter (OUS-RH). Det er anbefalt å vente minst to år etter transplantasjonen før svangerskap planlegges for å oppnå stabilitet og reduksjon av de immunsuppressive midlene. Immunsuppressive midler må tas kontinuerlig under svangerskapet, og serumkonsentrasjonen bestemmes og dosejusteres.
Om Nasjonal behandlingstjeneste for hjertesyke gravide ved Oslo Universitetssykehus Rikshospitalet
Nasjonal Behandlingstjeneste for hjertesyke gravide er en tverrfaglig tjeneste som er ansvarlig for utredning og behandling av hjertesyke gravide med høy risiko (mWHO klasse IV, se Tabell 1). Pasienter som faller inn i denne kategorien skal henvises behandlingstjenesten for svangerskapsoppfølging og fødsel. Utover denne henvisningsplikten, er det opp til de enkelte regionssykehusene selv å vurdere hvorvidt de innehar den nødvendige kompetanse og tverrfaglige infrastruktur til å håndtere de resterende hjertesyke med moderat og lav risiko i svangerskapet. Nødvendig infrastruktur og kompetanse innebærer i denne sammenheng tilgang til kardiolog, gynekolog og anestesilege, som alle har kunnskap om graviditet og fødsel hos pasienter med hjertesykdom. Nasjonal behandlingstjeneste for hjertesyke gravide ved OUS er behjelpelig med råd, kontroller og eventuell overtagelse av oppfølging og behandling av pasienten dersom denne ikke kan sikres ved lokal- eller regionssykehus. Det samme gjelder om kvinnens tilstand endres underveis i svangerskapet fra lav – moderat risiko til høyrisikosvangerskap. Mer informasjon finnes her: https://oslo-universitetssykehus.no/fag-og-forskning/nasjonale-og-regionale-tjenester/nasjonal-behandlingstjeneste-for-hjertesyke-gravide
Referanser
1. Roos-Hesselink JW, Budts W, Walker F, De Backer JFA, Swan L. Organisation of care for pregnancy in patients with congenital heart disease. Heart (British Cardiac Society). 2017;103(23):1854-9.
2. Regitz-Zagrosek V, Roos-Hesselink JW, Bauersachs J, Blomstrom-Lundqvist C, Cifkova R. 2018 ESC Guidelines for the management of cardiovascular diseases during pregnancy. European heart journal. 2018;39(34):3165-241.
3. Nasjonal Behandlingstjeneste for hjertesyke gravide. https://oslo-universitetssykehus.no/fag-og-forskning/nasjonale-og-regionale-tjenester/nasjonal-behandlingstjeneste-for-hjertesyke-gravide (lest 2 september 2019)
4. Ruys TP, Roos-Hesselink JW, Pijuan-Domenech A, Vasario E, Gaisin IR. Is a planned caesarean section in women with cardiac disease beneficial? Heart (British Cardiac Society). 2015;101(7):530-6.
5. Stout KK DC, Aboulhosn JA, et al. 2018 AHA/ACC Guideline for Adults With Congenital Heart Disease: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines. Journal of the American College of Cardiology. 2018;Aug 18.
6. RCOG. Cardiac Disease and Pregnancy. 2011;Good practice no. 13.
7. Cantwell R, Clutton-Brock T, Cooper G, Dawson A, Drife J. Saving Mothers' Lives: Reviewing maternal deaths to make motherhood safer: 2006-2008. The Eighth Report of the Confidential Enquiries into Maternal Deaths in the United Kingdom. BJOG : an international journal of obstetrics and gynaecology. 2011;118 Suppl 1:1-203.
8. Knight M BK, Tuffnell D, Jayakody H, Shakespeare J, Kotnis R.(Eds.) on, MBRRACE-UK. bo. Saving Lives, Improving Mothers’ Care - Lessons learned to inform maternity care from the UK and Ireland Confidential Enquiries into Maternal Deaths and Morbidity 2014-16. Oxford: National Perinatal Epidemiology Unit, University of Oxford 2018.
9. Pijuan-Domenech A, Galian L, Goya M, Casellas M, Merced C.Cardiac complications during pregnancy are better predicted with the modified WHO risk score. Int J Cardiol. 2015;195:149-54.
10. Thorne S, MacGregor A, Nelson-Piercy C. Risks of contraception and pregnancy in heart disease. Heart (British Cardiac Society). 2006;92(10):1520-5.
11. Emmanuel Y, Thorne SA. Heart disease in pregnancy. Best practice & research Clinical obstetrics & gynaecology. 2015;29(5):579-97.
12. Cauldwell M, Steer PJ, Swan L, Uebing A, Gatzoulis MA. The management of the third stage of labour in women with heart disease. Heart (British Cardiac Society). 2017;103(12):945-51.
13. Kinsella SM, Carvalho B, Dyer RA, Fernando R, McDonnell N. International consensus statement on the management of hypotension with vasopressors during caesarean section under spinal anaesthesia. Anaesthesia. 2018;73(1):71-92.
14. Langesaeter E, Dragsund M, Rosseland LA. Regional anaesthesia for a Caesarean section in women with cardiac disease: a prospective study. Acta anaesthesiologica Scandinavica. 2010;54(1):46-54.
15. Arendt KW, Lindley KJ. Obstetric anesthesia management of the patient with cardiac disease. International journal of obstetric anesthesia. 2019;37:73-85.
16. Habib G, Lancellotti P, Antunes MJ, Bongiorni MG, Casalta JP. [2015 ESC Guidelines for the management of infective endocarditis]. Kardiol Pol. 2015;73(11):963-1027.
17. Thorne S, Nelson-Piercy C, MacGregor A, Gibbs S, Crowhurst J.Pregnancy and contraception in heart disease and pulmonary arterial hypertension. The journal of family planning and reproductive health care. 2006;32(2):75-81.
18. Vigl M, Kaemmerer M, Niggemeyer E, Nagdyman N, Seifert-Klauss V.Sexuality and reproductive health in women with congenital heart disease. Am J Cardiol. 2010;105(4):538-41.
19. Hilfiker-Kleiner D, Haghikia A, Berliner D, Vogel-Claussen J, Schwab J.Bromocriptine for the treatment of peripartum cardiomyopathy: a multicentre randomized study. European heart journal. 2017;38(35):2671-9.