Anbefaler
• Utredning og oppfølging av dysplasi i svangerskap bør skje hos gynekolog med høy kompetanse innen kolposkopi. Målet med kolposkopi i svangerskapet er å utelukke cancer.
• Gravide kvinner anbefales å følge screeningprogrammet på lik linje med ikke gravide kvinner.
• Gravide kvinner med lavgradige celleforandringer følges som i screeningprogrammet.
• Ved mistanke om CIN2+, anbefales biopsi.
• Ved senere cytologisk/histologisk mistanke om invasiv lesjon eller forverret kolposkopisk bilde, anbefales nye biopsier.
• Kvinner som får cytologisk påvist ASC-H/HSIL/AGUS/AIS, eller har histologisk verifisert CIN 2/3 eller AIS, og blir gravide før behandling, eller får påvist dette under graviditet, følges med kolposkopi/cytologi og eventuelt biopsi hver 12. uke.
• Som hovedregel skal CIN 2/3 og AIS ikke behandles før etter svangerskapet
• Første postpartum kontroll med cytologi, kolposkopi, eventuelt biopsi (hvis indikasjon) anbefales ca 12 uker etter fødsel 1. Kontroll tidligere ved mistanke om mikroinvasiv cancer og AIS.
Anbefaler ikke
• Cervical abrasio frarådes i svangerskapet 1.
Forkortelser
Forklaring (norsk oversettelse)
AGUS
Atypical Glandular cells of Undetermined Significance (Atypisk sylinderepitel av usikker betydning (usikkert benignt/ malignt))
AIS/ACIS
Adenocarcinoma In Situ (Høygradige intraepiteliale forandringer i sylinderepitel/Adenokarsinom in situ)
ASC-H
Atypical Squamous Cells cannot exclude HSIL (Atypisk plateepitel, der høygradige celleforandringer i plateepitelet ikke kan utelukkes (usikkert benignt/ malignt))
ASC-US
Atypical Squamous Cells of Undetermined Significance (Atypisk plateepitel av usikker betydning)
CIN
Cervikal Intraepithelial Neoplasia (Cervixdysplasi;(histologisk diagnose) inkluderer: CIN1 (lette celleforandringer), CIN2 (moderate celleforandringer), CIN3 (grove celleforandringer), CIN2+ (moderate og grove celleforandringer eller kreft)
HPV
Human Papilloma Virus
LSIL
Low grade Squamous Intraepithelial Lesion (Lavgradige intraepiteliale forandringer i plateepitel)
HSIL
High grade Squamous Intraepithelial Lesion (Høygradige intraepiteliale forandringer i plateepitel)
Metaplasi
Fysiologisk og normal omdanning og dekning av sylinderepitel med plateepitel
Forekomst/epidemiologi
Globale prevalenstall for gravide er i stor grad avhengig av om det er etablert screening-program i den aktuelle befolkningsgruppe.
Risikoen for at CIN3 i løpet av svangerskapet progredierer til cervixcancer er ikke større hos gravide enn hos ikke gravide kvinner, og er rapportert å være 0,3 % 1.
Etiologi/patogenese
Persisterende infeksjon med høyrisiko HPV-genotype er en nødvendig forutsetning for utvikling av CIN og cervixcancer 2-5. Høyrisikotypene 16, 18, 31, 33, 45, 52, 58, er påvist i over 80-90% av CIN 2+ 6-8.
Faktorer assosiert med økt risiko for CIN2+
• Røyking 9-13
• Nedsatt immunforsvar (HIV-infeksjon/AIDS, SLE, immunsuppresjon) 10 14 15
• Tidlig seksuell debutalder og høyt antall seksualpartnere 16-18
• Langvarig bruk av P-piller 10 17 19
• Samtidig infeksjon med Chlamydia trachomatis 20
• Arvelige faktorer som HLA-type kan ha betydning for utvikling av CIN2+ 21
Diagnostikk av CIN
Symptomer: generelt ingen, evt. blødning fra ødematøse, hyperemiske slimhinner.
Gynekologisk undersøkelse: som oftest normal.
Mistanke om CIN oppstår etter cytologisk prøve fra cervix, diagnosen verifiseres ved biopsi.
Kolposkopi: Kan være vanskelig ved graviditet pga. øket vaskularisering, metaplasi, protruderende vaginalvegger og evt. desidualisering. Et avklippet kondom som trekkes over spekelet kan lette undersøkelsen.
Ved mistanke om CIN2+ anbefales biopsi (vurder å benytte liten biopsitang pga blødningsrisiko).
Nye og eventuelt større biopsier i graviditeten er aktuelt ved cytologisk/histologisk mistanke om cancer eller forverret kolposkopisk bilde.
Cervical abrasio: Frarådes i svangerskapet 1.
Spesielt hos gravide
• Gravide kvinner fra og med 25 år anbefales å ta livmorhalsprøve iht. retningslinjer gitt av Livmorhalsprogrammet.
• Gravide med lavradige celleforandringer kontrolleres etter anbefalingene i Livmorhalsprogrammet som hos ikke-gravide.
• Kvinner som får cytologisk påvist ASC-H/HSIL/AGUS/AIS, eller har histologisk verifisert CIN 2/3 eller AIS og blir gravide før behandling, eller får påvist dette under graviditet, følges med kolposkopi/cytologi og eventuelt biopsi hver 12. uke 1.
• Gravide som følges opp under svangerskapet pga. tidligere langvarige usikre eller lavgradige celleforandringer, og som ikke viser progresjon i cytologisk prøve – avvent vurdering med biopsi til etter svangerskapet.
• Første postpartum kontroll med kolposkopi, cytologi og HPV test anbefales 12 uker etter fødsel 1 hos erfaren kolposkopist. Vi anbefaler tidligere kontroll ved mistanke om microinvasiv cancer eller AIS.
- Dersom cytologisk og/ eller histologisk verifisert høygradig dysplasi, før eller i svangerskapet, anbefales det vevsprøver ved 12 ukers kontrollen.
- Ved histologisk verifisert høygradig dysplasi før eller i svangerskapet og klare kolposkopiske funn forenelig med høygradig dysplasi eller microinvasiv cancer, bør man vurdere å gå rett på konisering.
Dersom cytologisk lavgradige funn før eller i svangerskapet ikke har blitt biopsert etter retningslinjene, fordi pasienten var gravid, kan dette gjøres ved 12 ukers kontrollen post partum i tillegg til cytologi og HPV-testing.
• OBS: Atypisk sylinderepitel i cytologisk prøve kan indikere atypisk intraepitelialt sylinderepitel (AIS), adenocarcinom i cervix eller endometriecancer, noe som er vanskelig å bekrefte histologisk i graviditeten.
Differensialdiagnostikk til CIN
• Irregulær metaplasi
• Graviditetsbasert hypertrofi
• Kondylomer
• Cancer cervicis uteri
• Seksuelt overført sykdom (STD) /genitale infeksjonssykdommer
Forløp/ tiltak/behandling av preinvasive lesjoner (CIN2/CIN3/ACIS)
Risiko for progresjon av CIN2+ til invasiv kreft i graviditet er minimal (0,3 %), og spontan regresjon av CIN2/CIN3 etter fødsel er sett i 30-70 %1. Derfor utføres konisering i svangerskapet bare dersom man er usikker på om det foreligger invasiv kreft1.
Generelt har man til nå vært svært tilbakeholden med konisering i graviditet, da cervix i større grad er vaskularisert. Dette kan øke risikoen for per- og postoperativ blødning, som igjen kan øke infeksjonsfaren og risikoen for abort. Det finnes kun et fåtall av studier som omhandler konisering i tidlig svangerskap 22, og i de fleste sammenlignbare land gjøres konisering i graviditet kun ved mistanke om cervixcancer eller påvist tidlig mikroinvasiv cancer. I Norge bør dette sentraliseres.
Vaginal forløsning kan øke regresjonsraten av CIN sammenliknet med kvinner forløst med keisersnitt 23. Ny kolposkopi og nye kolposkopisk rettede biopsier 12 uker postpartum anbefales (tidligere ved mistanke om invasivitet). Hvis prøvesvarene fortsatt viser CIN2+, utføres konisering.
Forløp/ tiltak/behandling av invasiv cervixcancer
Cervixcancer under graviditet er en sjelden tilstand og behandlingen er sentralisert til regionssykehus. Behandlingen er individualisert, der behandlingsprinsippene for ikke-gravide følges mest mulig.
Kvinnen kan ha symptomer i form av vaginal blødning eller illeluktende fluor. Alle gravide kvinner med slike symptomer må undersøkes gynekologisk med inspeksjon av portio. Bare ultralydundersøkelse er ikke tilstrekkelig ved vaginalblødning/illeluktende, blodig fluor. Erfaringsmessig blir diagnosen ofte forsinket, fordi man ikke tenker på dette.
Pasienten henvises som øyeblikkelig hjelp til avdeling/seksjon for gynekologisk onkologi. Pasienten må få full informasjon om tilstanden, slik at hun også kan være med på å ta standpunkt til selve behandlingen.
Invasiv cervixcancer i første trimester og til utgangen av 19. svangerskapsuke
Hvis kvinnen har et ønske om å beholde sin graviditet, kan hun trygt gjøre det ved tidlig cancer. Hvis det ikke foreligger et ønske om å fullføre graviditeten, avbrytes den, og kvinnen behandles etter vanlige prinsipper. Ved funn av lymfeknutemetastaser eller stadium IIB eller over, anbefales det å avslutte graviditeten.
Ved stadium IA1 uten karinfiltrasjon kan pasienten behandles med konisering i uke 14-20. For stadium IA1 med karinfiltrasjon og stadium IA2 samt IB1 anbefales lymfeknutetoalett, og ved små svulster kan noen av disse også koniseres. Der konisering ikke er et bra alternativ, kan pasienten behandles med neoadjuvant kjemoterapi eller observeres og behandles ved fullgått graviditet. Stadium IB2 og IB3 behandles med neoadjuvant kjemoterapi og behandles ferdig etter fødsel 24.
Svangerskapsvarighet mellom utgangen av 19. svangerskapsuke og til 24. fullgåtte uke
En svært vanskelig avveining: Skal svangerskapet avbrytes og behandling iverksettes, eller skal man vente til fosteret er levedyktig før behandling startes?
Pasienten henvises til regionssykehus eller DNR. Behandlingen er individualisert, men gjøres på samme prinsipper som skisseres ovenfor.
Hvis konklusjonen blir at svangerskapet avbrytes, blir behandlingsopplegget tilsvarende som hos ikke gravide pasienter. Ved fortsatt graviditet blir behandling utsatt, eller det blir gitt neoadjuvant kjemoterapi henhold til prinsipper nevnt over.
Svangerskapsvarighet etter 24. fullgåtte uke
Graviditeten avbrytes ikke etter uke 24. Pasienter i stadium IA1 til IB1 kan følges uten behandling med kontroller hver 4. uke. Fødsel skal ikke settes i gang, og pasienten bør forløses med sectio ved fullgått svangerskap. Stadium IB2 eller over behandles med neoadjuvant kjemoterapi frem til uke 35-36 og forløses med sectio ved fullgått svangerskap. I noen tilfeller gjøres radikal hysterektomi og lymfeknutetoalett i forbindelse med sectio.
Komplikasjoner etter konisering
Norske studier har vist økt risiko for preterm fødsel etter konisering med høyest relativ risiko ved lavere gestasjonsalder og økt mengde cervixvev fjernet 25 26, samt 4 ganger økt risiko for senabort 27.
Studier fra England viser at risikoen for prematur fødsel i den generelle befolkningen der er 6,7%
28
. Hos kvinner med CIN uten gjennomgått konisering, øker risikoen for prematur fødsel til 7,2%. Risikoen for prematur fødsel hos kvinner som er konisert med en lav kon (<10 mm) og de som kun er biopsert er tilsvarende (7,5% vs 7,2%)
29
. Risikoen for prematur fødsel øker med økende dybde og volum av kon preparatet, som vist i tabellen under
29 30
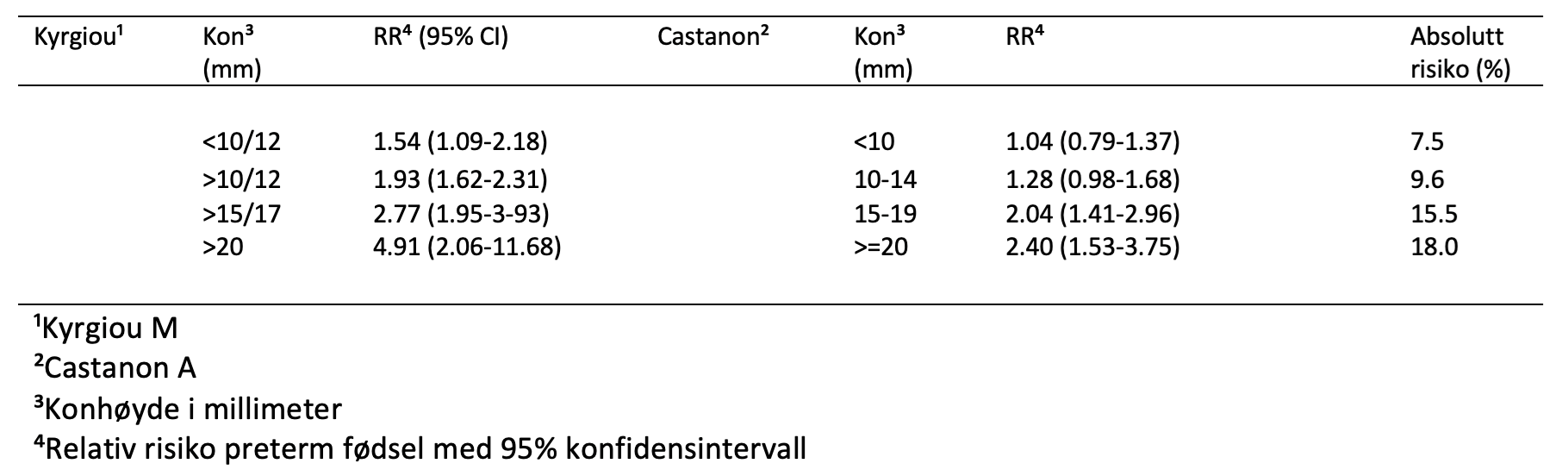
På grunnlag av disse tallene anbefales følgende:
Koniserte trenger ikke spesiell oppfølging i første svangerskap etter konisering med mindre de har senabort eller prematur fødsel i tidligere sykehistorie. Ved gjentatte koniseringer eller konhøyde >= 20 mm, vurder henvisning til fødepol i svangerskapsuke 16-24 for ultralydmåling av cervixlengde, se forøvrig kapittel «Preterm fødsel».
Pasientinformasjon
Pasientinformasjon ved CIN:
• Informasjon om HPV og celleforandringer finner pasienten på Kreftregisterets hjemmesider/ Livmorhalsprogrammet
• Informasjon gitt av lege bør inneholde:
- Forklaring på hva celleforandringer er; bruk celleforandringer, ikke «kreftceller», unngå ”alvorlige” celleforandringer
- At HPV-infeksjon i seg selv ikke er farlig, at HPV og celleforandringer er svært vanlig og ofte går over av seg selv og at eventuell utvikling til livmorhalskreft går over mange år
- Hva som skal følges opp i graviditeten, kontrollen postpartum og eventuell operasjon
- Generell informasjon om konisering
- Hvorfor vi ikke gjør konisering under graviditeten
Pasientinformasjon ved cervixcancer:
- Må individualiseres
- Behandlingsprinsippene for ikke-gravide følges så langt mulig
- Pasientene henvises gynekologisk onkologisk avdeling
Søkeord for app versjonen:
celleforandringer, svangerskap, for tidlig fødsel, prematur fødsel, svangerskap, LSIL, HSIL, CIN1, CIN2, CIN3, AIS
Vurdering av dokumentasjon/ Søkestrategi
Det er utført ikke-systematiske litteratursøk i PubMed, Goolge Scholar og via referanser i siterte artikler. Anbefalingene er videre basert på svenske retningslinjer og ekspertuttalelser
Emneord
Low-grade squamous intraepithelial lesions (LSIL)
High-grade squamous intraepithelial lesions (HSIL)
Cervical intraepithelial neoplasia (CIN)
Cervical preinvasive disease
Cervical cancer
Pregnancy
Adverse obstetric outcomes
Preterm birth
Referanser
1. Hunter MI, Monk BJ, Tewari KS. Cervical neoplasia in pregnancy. Part 1: screening and management of preinvasive disease. American journal of obstetrics and gynecology 2008;199(1):3-9. doi: 10.1016/j.ajog.2008.04.010 [published Online First: 2008/07/01]
2. Munoz N, Bosch FX, de Sanjose S, et al. Epidemiologic classification of human papillomavirus types associated with cervical cancer. The New England journal of medicine 2003;348(6):518-27. doi: 10.1056/NEJMoa021641 [published Online First: 2003/02/07]
3. Walboomers JM, Jacobs MV, Manos MM, et al. Human papillomavirus is a necessary cause of invasive cervical cancer worldwide. The Journal of pathology 1999;189(1):12-9. doi: 10.1002/(sici)1096-9896(199909)189:1<12::aid-path431>3.0.co;2-f [published Online First: 1999/08/19]
4. Bosch FX, Broker TR, Forman D, et al. Comprehensive control of human papillomavirus infections and related diseases. Vaccine 2013;31 Suppl 7:H1-31. doi: 10.1016/j.vaccine.2013.10.003 [published Online First: 2013/12/18]
5. IARC. Monographs on the evaluation of carcinogenic risks to humans, vol 100B, p. 255-296 Lyon: IARC; 2012 [cited 2018 03.09.]. Available from: https://monographs.iarc.fr/wp-content/uploads/2018/06/mono100B-11.pdf accessed 03.09. 2018.
6. Smith JS, Lindsay L, Hoots B, et al. Human papillomavirus type distribution in invasive cervical cancer and high-grade cervical lesions: a meta-analysis update. International journal of cancer 2007;121(3):621-32. doi: 10.1002/ijc.22527 [published Online First: 2007/04/04]
7. Tjalma WA, Fiander A, Reich O, et al. Differences in human papillomavirus type distribution in high-grade cervical intraepithelial neoplasia and invasive cervical cancer in Europe. International journal of cancer 2013;132(4):854-67. doi: 10.1002/ijc.27713 [published Online First: 2012/07/04]
8. Arbyn M, Tommasino M, Depuydt C, et al. Are 20 human papillomavirus types causing cervical cancer? The Journal of pathology 2014;234(4):431-5. doi: 10.1002/path.4424 [published Online First: 2014/08/16]
9. Vaccarella S, Herrero R, Snijders PJ, et al. Smoking and human papillomavirus infection: pooled analysis of the International Agency for Research on Cancer HPV Prevalence Surveys. International journal of epidemiology 2008;37(3):536-46. doi: 10.1093/ije/dyn033 [published Online First: 2008/03/05]
10. Gadducci A, Barsotti C, Cosio S, et al. Smoking habit, immune suppression, oral contraceptive use, and hormone replacement therapy use and cervical carcinogenesis: a review of the literature. Gynecological endocrinology : the official journal of the International Society of Gynecological Endocrinology 2011;27(8):597-604. doi: 10.3109/09513590.2011.558953 [published Online First: 2011/03/29]
11. Appleby P, Beral V, Berrington de Gonzalez A, et al. Carcinoma of the cervix and tobacco smoking: collaborative reanalysis of individual data on 13,541 women with carcinoma of the cervix and 23,017 women without carcinoma of the cervix from 23 epidemiological studies. International journal of cancer 2006;118(6):1481-95. doi: 10.1002/ijc.21493 [published Online First: 2005/10/06]
12. Kapeu AS, Luostarinen T, Jellum E, et al. Is smoking an independent risk factor for invasive cervical cancer? A nested case-control study within Nordic biobanks. American journal of epidemiology 2009;169(4):480-8. doi: 10.1093/aje/kwn354 [published Online First: 2008/12/17]
13. Roura E, Castellsague X, Pawlita M, et al. Smoking as a major risk factor for cervical cancer and pre-cancer: results from the EPIC cohort. International journal of cancer 2014;135(2):453-66. doi: 10.1002/ijc.28666 [published Online First: 2013/12/18]
14. Grulich AE, van Leeuwen MT, Falster MO, et al. Incidence of cancers in people with HIV/AIDS compared with immunosuppressed transplant recipients: a meta-analysis. Lancet (London, England) 2007;370(9581):59-67. doi: 10.1016/s0140-6736(07)61050-2 [published Online First: 2007/07/10]
15. Jordan J, Martin-Hirsch P, Arbyn M, et al. European guidelines for clinical management of abnormal cervical cytology, part 2. Cytopathology : official journal of the British Society for Clinical Cytology 2009;20(1):5-16. doi: 10.1111/j.1365-2303.2008.00636.x [published Online First: 2009/01/10]
16. International Collaboration of Epidemiological Studies of Cervical Cancer. Comparison of risk factors for invasive squamous cell carcinoma and adenocarcinoma of the cervix: collaborative reanalysis of individual data on 8,097 women with squamous cell carcinoma and 1,374 women with adenocarcinoma from 12 epidemiological studies. International journal of cancer 2007;120(4):885-91. doi: 10.1002/ijc.22357 [published Online First: 2006/11/30]
17. International Collaboration of Epidemiological Studies of Cervical Cancer. Cervical carcinoma and sexual behavior: collaborative reanalysis of individual data on 15,461 women with cervical carcinoma and 29,164 women without cervical carcinoma from 21 epidemiological studies. Cancer epidemiology, biomarkers & prevention : a publication of the American Association for Cancer Research, cosponsored by the American Society of Preventive Oncology2009;18(4):1060-9. doi: 10.1158/1055-9965.Epi-08-1186 [published Online First: 2009/04/02]
18. Dillner J, Kallings I, Brihmer C, et al. Seropositivities to human papillomavirus types 16, 18, or 33 capsids and to Chlamydia trachomatis are markers of sexual behavior. The Journal of infectious diseases 1996;173(6):1394-8. doi: 10.1093/infdis/173.6.1394 [published Online First: 1996/06/01]
19. Smith JS, Green J, Berrington de Gonzalez A, et al. Cervical cancer and use of hormonal contraceptives: a systematic review. Lancet (London, England) 2003;361(9364):1159-67. doi: 10.1016/s0140-6736(03)12949-2 [published Online First: 2003/04/11]
20. Silins I, Ryd W, Strand A, et al. Chlamydia trachomatis infection and persistence of human papillomavirus. International journal of cancer 2005;116(1):110-5. doi: 10.1002/ijc.20970 [published Online First: 2005/03/10]
21. Leo PJ, Madeleine MM, Wang S, et al. Defining the genetic susceptibility to cervical neoplasia-A genome-wide association study. PLoS genetics 2017;13(8):e1006866. doi: 10.1371/journal.pgen.1006866 [published Online First: 2017/08/15]
22. Siegler E, Amit A, Lavie O, et al. Cervical intraepithelial neoplasia 2, 3 in pregnancy: time to consider loop cone excision in the first trimester of pregnancy? Journal of lower genital tract disease 2014;18(2):162-8. doi: 10.1097/LGT.0b013e318299c0af [published Online First: 2013/09/03]
23. Ueda Y, Enomoto T, Miyatake T, et al. Postpartum outcome of cervical intraepithelial neoplasia in pregnant women determined by route of delivery. Reproductive sciences (Thousand Oaks, Calif) 2009;16(11):1034-9. doi: 10.1177/1933719109339349 [published Online First: 2009/07/01]
24. Amant F, Berveiller P, Boere I, et al. Gynecologic cancers in pregnancy: guidelines based on a third international consensus meeting. Annals of oncology : official journal of the European Society for Medical Oncology 2019 doi: 10.1093/annonc/mdz228 [published Online First: 2019/08/23]
25. Sjoborg KD, Vistad I, Myhr SS, et al. Pregnancy outcome after cervical cone excision: a case-control study. Acta obstetricia et gynecologica Scandinavica 2007;86(4):423-8. doi: 10.1080/11038120701208158 [published Online First: 2007/05/09]
26. Bjorge T, Skare GB, Bjorge L, et al. Adverse Pregnancy Outcomes After Treatment for Cervical Intraepithelial Neoplasia. Obstetrics and gynecology 2016;128(6):1265-73. doi: 10.1097/aog.0000000000001777 [published Online First: 2016/11/09]
27. Albrechtsen S, Rasmussen S, Thoresen S, et al. Pregnancy outcome in women before and after cervical conisation: population based cohort study. BMJ (Clinical research ed) 2008;337:a1343. doi: 10.1136/bmj.a1343 [published Online First: 2008/09/20]
28. Castanon A, Brocklehurst P, Evans H, et al. Risk of preterm birth after treatment for cervical intraepithelial neoplasia among women attending colposcopy in England: retrospective-prospective cohort study. BMJ (Clinical research ed)2012;345:e5174. doi: 10.1136/bmj.e5174 [published Online First: 2012/08/18]
29. Castanon A, Landy R, Brocklehurst P, et al. Risk of preterm delivery with increasing depth of excision for cervical intraepithelial neoplasia in England: nested case-control study. BMJ (Clinical research ed) 2014;349:g6223. doi: 10.1136/bmj.g6223 [published Online First: 2014/11/08]
30. Kyrgiou M, Athanasiou A, Paraskevaidi M, et al. Adverse obstetric outcomes after local treatment for cervical preinvasive and early invasive disease according to cone depth: systematic review and meta-analysis. BMJ (Clinical research ed)2016;354:i3633. doi: 10.1136/bmj.i3633 [published Online First: 2016/07/30]