Revidert 24. april 2022
Første versjon 16. februar 2020
Anbefalinger
Vi anbefaler at det foreligger en medisinsk indikasjon for igangsettelse av fødsel (II).
Vi foreslår at fødeinstitusjoner følger en standard protokoll for igangsettelse av fødsel, basert på modenhetsgrad av livmorhalsen og kvinnens Robson 10-gruppe (IV).
Vi anbefaler at livmorhalsen strippes ved kontroll etter termin (I).
Vi anbefaler at fødeinstitusjoner utarbeider skriftlig informasjon til kvinner som skal ha igangsettelse av fødsel (I).
Vi anbefaler at kvinner som igangsettes enten med prostaglandin eller oksytocin overvåkes nøye (I).
Vi foreslår at følgende bør være i avdelingen etter igangsettelse av fødsel (IV):
Kvinner med moderat/alvorlig preeklampsi, insulinkrevende diabetes mellitus, flerlingsvangerskap, seteleie hos foster, tidligere keisersnitt, induksjon ved prematuritet, veksthemmet foster, der det foreligger oligohydramnion eller anhydramnion, PROM, lang reisevei eller kommunikasjons/språkvansker.
Søkestrategi
Pyramidesøk McMaster PLUS (via Helsebiblioteket.no), UpToDate, PubMed, Cochrane Database, American College of Obstetricians and Gynecologists (ACOG), Royal College of Obstetricians and Gynecologists (RCOG), World Health Organization (WHO). Søkeord “induction of labour/labor”, “cervical ripening”, “systematic review”, and “meta-analysis”.
Søkeord for app-versjonen
Induksjon – igangsetting - modning – cervix - livmorhals
Definisjon
Kunstig igangsetting (induksjon) av fødsel, der det grunnet maternell eller føtal indikasjon er ønskelig å avslutte svangerskapet, og hvor det ikke foreligger kontraindikasjoner mot vaginal fødsel. Verdens helseorganisasjon (WHO) anbefaler at igangsettelse av fødsel utføres med en klar medisinsk indikasjon og når fordelene for mor eller barn antas større enn risikoen ved å fortsette svangerskapet. [1]
Fysiologi
Modning av livmorhalsen
Prosessen der en lang, fast (kollagenrik), lukket livmorhals forvandles til en kortere, mykere og åpnere livmorhals. Hos gravide skjer dette fysiologisk før spontan fødselsstart. Den eksakte mekanismen som fører til livmorhalsmodning er ikke kjent. Den fysiologiske modningsprosessen kan inndeles i fire stadier, men flere stadier kan foregå parallelt:
- Vevet blir mykt ved at kollagenfibrenes mengde og struktur endrer seg. En langsom prosess, som antas å foregå over dager/uker.
- Prostaglandinkaskaden aktiveres. Dette fører til en inflammasjon i livmorhalsvevet. Dette stadiet foregår raskere og antas å ta timer/dager. Man tror at økt prostaglandindannelse forårsaker omsettingen og reguleringen av kollagen i livmorhals.[2]
- Livmorhalsen dilaterer seg i løpet av timer.
- Etter fødselen gjenoppbygges vevet i livmorhalsen tilbake til den opprinnelige strukturen.
Igangsetting av fødsel: forekomst
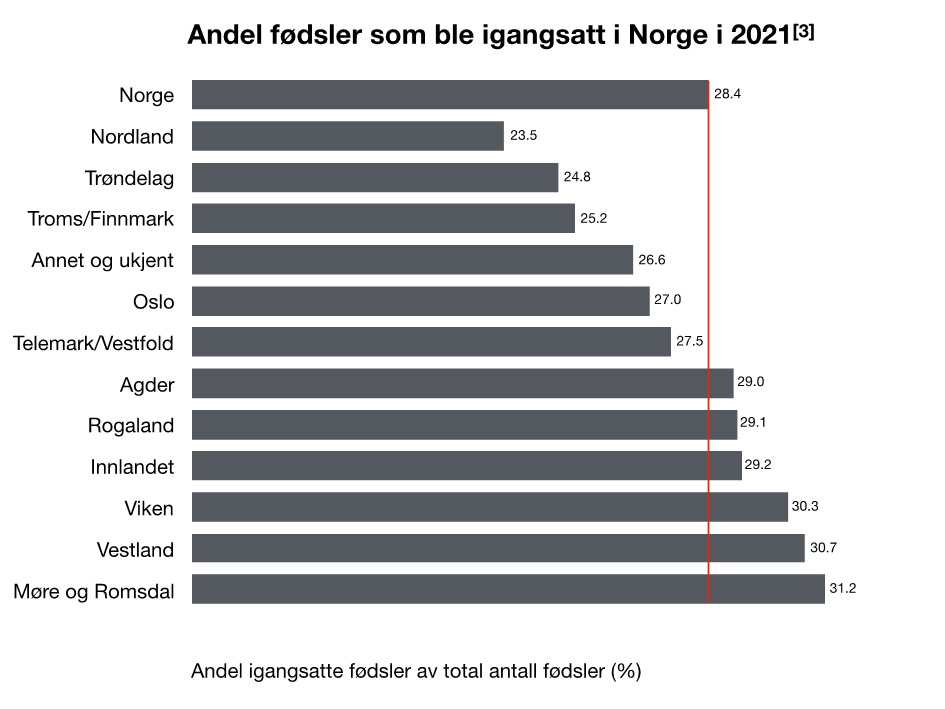
Andelen og antall igangsatte fødsler i Norge har økt kraftig de siste 20 år. I 2000 var andel igangsatte fødsler 8.8%. I 2021 var tallet 28.4.[3] Det er forskjell mellom helseregioner og fødeinstitusjoner. Ved enkelte fødeinstitusjoner nærmer andel igangsatte fødsler seg en tredjedel av alle fødsler (Den norske induksjonsstudien, 2018).[4] Keisersnittsfrekvensen for alle fødsler har vært stabil mellom 2003 (15,4%) og 2021 (15.6%), til tross for den sterke økningen i antall induksjoner.[5]
Forskjeller mellom fødeinstitusjoner kan ha mange forklaringer:
Tilfeldigheter, ulik bruk av diagnostiske kriterier, risikosentralisering, variasjoner i fødejournalsystemenes data, variasjon i meldepraksis og meldesvikt, reelle forskjeller i kvalitet. MFR data er basert på tall innhentet fra Natus/Partus – ikke alle fødeavdelinger registrerer all obstetrisk utkomme Natus/Partus. Det er ofte en kombinasjon av flere faktorer.[6]
Internasjonalt er det meget stor variasjon av forekomst igangsatte fødsler, med lavest andel i ressurssvake land (f.eks. 1.4% i Niger)[7] og høyest andel i ressurssterke land (hver tredje kvinne i Italia[8]).
I en nasjonal registrering med 21 norske fødeinstitusjoner i 2018[4] ble det registrert over 40 ulike metoder (kombinasjoner) for igangsetting av fødsel. De hyppigste indikasjoner, uavhengig av Robson 10 gruppe, for kvinner uten tidligere vaginal fødsel:
- Vannavgang uten rier: 19.6 %
- Etter termin/overtidig svangerskap: 18.5%
- Hypertensjon/preeklampsi: 15.2%
- Oligohydramnion: 7.9%
- Veksthemmet foster: 7.5%
- Diabetes (alle typer, inkludert kostregulert): 7.3%
Indikasjoner og kontraindikasjoner for igangsetting
Steroider for lungemodning skal gis ved igangsetting før svangerskapsuke 34+0. Kfr. kapittel ”Truende for tidlig fødsel”.
Alle igangsettinger bør ha en indikasjon, og indikasjonsstillingen bør være dokumentert i journalen.
Eksempler på medisinske Indikasjoner
- Overtidig svangerskap (Evidensnivå I) [9],[10]
- Preeklampsi/hypertensjon/PIH (Pregnancy Induced Hypertension) (I)[11]
- Pregestasjonell diabetes mellitus I og II, (IV)[12],[13]
- Svangerskapsdiabetes, insulinavhengig (IV)
- Primær vannavgang etter 37 uker (I) [14],[15]
- Tvillingsvangerskap (IV)[16],[17]
- Intrahepatisk svangerskapskolestase (II)[18]
- Andre medisinske indikasjoner.
Anmerkning vedrørende overtidig svangerskap i Cochrane-anbefalingen om induksjon ved termin eller etter termin i lav-risiko svangerskap: en av svakhetene ved Cochrane-analysen at den inkluderer studier fra land med høyere forekomst av intrauterin fosterdød enn Skandinavia. Siden det allerede er en lav forekomst av intrauterin fosterdød i Skandinaviske land, kan sykeliggjøring av en stor gruppe lavrisiko svangerskap ikke nødvendigvis føre til noen gevinst og kan i verste fall gjøre mer skade enn nytte.
En stor retrospektiv kohort undersøkelse fra Danmark (2019)10 har undersøkt forskjeller i neonatale utfall etter at det i 2011 ble anbefalt endring ved rutinemessig fødselsinduksjon i svangerskap etter termin. I Danmark ble det før 2011 anbefalt rutinemessig fødselsinduksjon ved svangerskapsuke 42+0, men i 2011 ble anbefalingene endret til rutinemessig induksjon fra uke 41+3 til 41+5. Studien, som undersøkte mer enn 152 000 fødsler med svangerskapslengde mellom 41+4 og 45+0 mellom 2000-2016, fant ingen forskjeller i neonatale utfall, inkludert intrauterin fosterdød, etter at fødselsinduksjon ble startet i svangerskapsuke 41+3, sammenlignet med fødselsinduksjon fra uke 42+0. Derimot førte fødselsinduksjon fra svangerskapsuke 41+3, sammenlignet med induksjon ved uke 42+0, til en signifikant økning i antall fødselsinduksjoner, fra 41% til 65%, økt bruk av epiduralbedøvelse, økt av bruk ristimulerende medisin, samt en dobling av uterusrupturer fra 2.6 til 4.2 per tusen fødsler.
Ved kostregulert svangerskapsdiabetes, der det kun foreligger diabetes som medisinsk problem, er igangsetting av fødsel ikke anbefalt (evidensnivå IV).11,[19]
Ved intrauterin tilveksthemming er det publisert få studier på utkomme ved igangsetting versus overvåkning.[20] En studie (2010) har ikke funnet fordeler ved igangsetting versus intensiv overvåking. [21] Det er heller ikke noen studier som kan vise fordeler ved igangsetting ved oligohydramnion/anhydramnion.
Ved mistenkt stort foster er det ingen konsensus om hvorvidt igangsetting av fødsel forebygger skulderdystoci eller annen ledsagende neonatal og/eller maternell morbiditet. En prospektiv studie fra Frankrike, Sveits og Belgia (2015) konkluderte at igangsetting forebygget tilfeller av skulderdystoci. 822 kvinner med singleton foster og estimert vekt over 95-percentilen (Large-for-Gestational age, LGA), ble inkludert.[22] Kvinnene ble randomisert til igangsetting av fødsel innen 3 dager mellom 37+0 uker og 38+6 uker av svangerskapet, eller kun overvåking til spontan fødselsstart (2002-2009). Det var 8 tilfeller av skulderdystoci i induksjonsgruppen versus 25 tilfeller i gruppen med spontan fødselsstart. En retrospektiv svensk fødselsregisterstudie (2017) fant ingen forskjell i skulderdystoci mellom 722 kvinner med igangsatt fødsel i svangerskapsuke 38 for LGA-fostre, og kvinner med spontan fødselsstart.[23] Det var imidlertid økt forekomst av keisersnitt hos kvinnene som fikk fødselen igangsatt. En metaanalyse (2017) av tre små upubliserte studier om igangsetting ved makrosomt foster fant ikke redusert forekomst av skulderdystoci.[24]
Igangsetting uten medisinsk indikasjon
En studie fra 24 fødeinstitusjoner i Norge i 2013, fant at hver 10. igangsetting av fødsel er uten medisinsk indikasjon.[25] Kun 16% av kvinnene i studien var førstegangsfødende. «Eget ønske» fra kvinnen var den hyppigste årsaken. Andre årsaker var at kvinnen var sliten, engstelig, eller tidligere dårlig fødselsopplevelse. Av kvinnene som ble igangsatt uten medisinsk indikasjon, fødte 86% vaginalt. I valget mellom elektivt keisersnitt og igangsetting av fødsel på kvinnens forespørsel, uten annen medisinsk indikasjon, kan igangsetting være et fornuftig kompromiss, dersom kvinnen tidligere har født vaginalt.
Kontraindikasjoner til igangsetting av fødsel
- Alvorlig preeklampsi eller annen medisinsk tilstand hos mor eller foster der forløsning innen ønsket tid ikke kan forventes.
- Tegn på føtal distress ved CTG-registrering eller doppler hvor man har grunn til å tro at fosteret ikke har tilstrekkelige ressurser til å tåle vaginal forløsning.
- Annen maternell eller føtal kontraindikasjon for vaginal forløsning.
- Registrerte prostaglandiner som Angusta® og Propess® er kontraindisert ved tidligere keisersnitt eller kirurgi på uterus og har egne tilleggskontraindikasjoner – les pakningsvedlegget.
Ved igangsetting av fødsel foreslår vi at følgende kvinner innlegges: Kvinner med moderat preeklampsi, insulinkrevende diabetes mellitus, flerlingsvangerskap, seteleie hos foster, tidligere keisersnitt, induksjon ved prematuritet, veksthemmet foster, der det foreligger oligohydramnion eller anhydramnion, PROM og for kvinner med lang reisevei.
Robson grupper[26] og igangsetting av fødsel
Se Figur 1 i referanse 26 for utførlig beskrivelse av Robson 10 gruppene.
Ved igangsettelse av fødsel til termin med ett foster i hodeleie har nullipara (Robson gruppe 2) en høyere risiko for mislykket igangsettelse og keisersnitt enn multipara (Robson gruppe 4). Kvinner som tidligere kun har vært forløst ved keisersnitt eller har arr i livmoren (Robson gruppe 5) har enda høyere risiko for mislykket igangsettelse enn kvinner i Robson gruppe 2 og 4.[27],[28],[29],[30],[31],[32],[33]
Vesentlig ved igangsetting er vurdering av modenhetsgraden til livmorhalsen med Bishops score. En norsk studie (2011) på igangsetting av fødsel i overtidige svangerskap fant at måling av livmorhalslengden med vaginal ultralyd var en viktig tilleggsundersøkelse, i tillegg til vurdering av Bishops score med fingrene.[34] I den norske induksjonsstudien i 20184 er det enkelte sykehus der modenhetsgraden til livmorhalsen ikke ble undersøkt før induksjon. Dette gjør at man ikke kan tilpasse igangsettelse og/eller informasjon om igangsettelse til kvinnen.
Merk at Bishop’s Score i sin tid ble utviklet for igangsetting av multipara uten svangerskapskomplikasjoner.[35] 50 år senere er den fortsatt det mest brukte verktøyet verden rundt til å vurdere igangsettingsmetoden. En forenklet metode med bare tre variabler har nylig vært brukt for å vurdere livmorhals før igangsetting av nullipara.[36] En fast, kollagenrik og lang livmorhals vil ta lengre tid å sette i gang sammenlignet med en myk, kollagenfattig og kort livmorhals (Den norske induksjonstudien 2018)4.
Det foreslås å bruke en høyere poengsum som grense for ”moden livmorhals” hos førstegangsfødende, enn hos flergangsfødende ved bruk av Bishop’s Score med 5 variabler.
Poengsum
>7: moden livmorhals hos nullipara – (Bishop’s score med 5 variabler)
> 5: moden livmorhals hos multipara med tidligere vaginal fødsel (Bishop’s score med 5 variabler)
FLYTSKJEMA
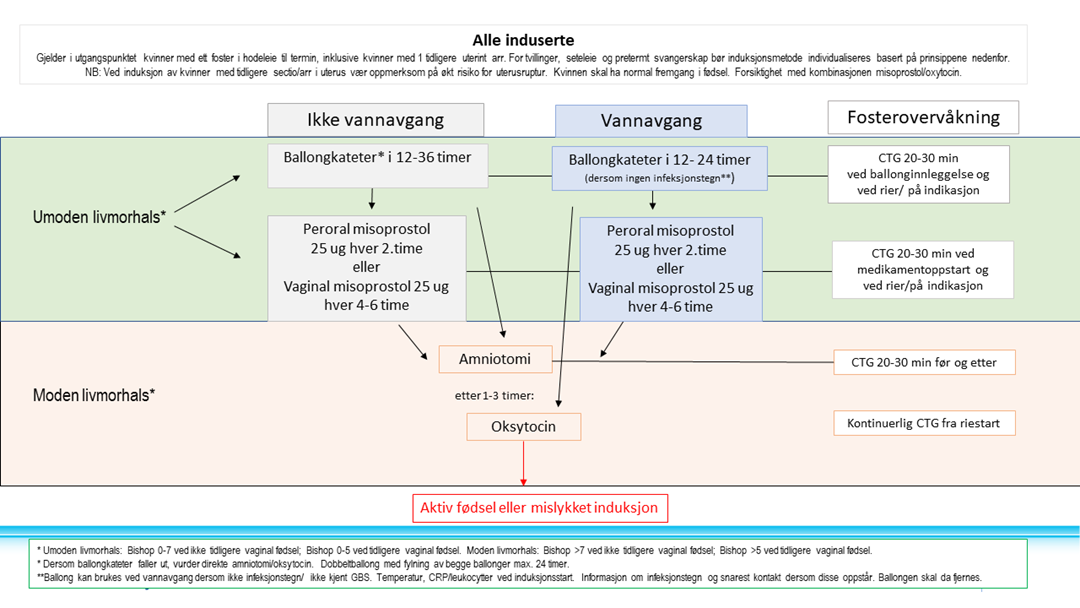
Pasientinformasjon
Det er viktig at den gravide i forkant får informasjon om behandlingen og forventet forløp ved modning av livmorhals/igangsetting av fødsel. Det anbefales at fødeavdelingen lager skriftlig pasientinformasjon tilpasset sykehusets rutiner (se vedlegg 1 «Pasientinformasjon igangsetting av fødsel»).
Protokoll for igangsettelse av fødsel
Vi anbefaler at alle fødeinstitusjoner utarbeider en standard protokoll for igangsettelse av fødsel, basert på kvinnens Robson 10 gruppe og modenhetsgrad av livmorhals. Avdelingens prosedyre bør ha en prioriteringsrekkefølge. Vi anbefaler at legen som starter induksjonen lager en tids- og behandlingsplan for kvinnen, helst skriftlig.
Forslag til lokal protokoll – se vedlegg 2 «Eksempel på lokal prosedyre»
Metoder
1. Mekanisk tøyning av livmorhals/”stripping”/hinneløsning (I)1
Mekanisk tøyning av livmorhals (”stripping of the membranes”) forårsaker økt phospholipase A2- og prostaglandin F2α aktivitet. Ved vaginalundersøkelse fører man inn pekefingeren gjennom indre mormunn. Livmorhalsen tøyes og strekkes og fosterhinner løsnes fra nedre uterinsegment ved at man dilaterer livmorhals med sirkulære bevegelser. Tøyning av livmorhals kan utføres mens kvinnen ligger på undersøkelsesbenk eller i benholdere i GU-stol. Det er ukjent hvor lenge man må tøye livmorhalsen for å starte/fremskynde modningsprosessen, vi anbefaler minst 20-30 sekunder, dersom det er mulig. Stripping av hinner anbefales ved svangerskapskontroller etter termin og er vist å redusere behovet for igangsetting med andre metoder (I).
Komplikasjoner
Ubehag for kvinnen og litt blødning er vanlig ved denne metoden.
2. Bruk av ballongkateter i livmorhals, f.eks. latex Foleykateter 22 Ch eller Cervical Ripening Balloon® (Cook) (I)[37]
Randomiserte kliniske studier som sammenligner kateter mot prostaglandiner viser at kateter er like effektivt som prostaglandiner til å indusere fødsel (I).[38] Igangsetting med kateter har flere tilleggsfordeler fremfor prostaglandiner. Det er lavere risiko for hyperstimulering av uterus med kateter og lavere risiko for mekoniumavgang fra foster (II). Mekanismen for livmorhalsmodning er ikke kjent, men man har fremmet teorien om at lokal vevsnekrose forårsaket av trykk fra kateteret igangsetter prostaglandin-kaskaden. Vaginal ultralyd kan med fordel brukes for å kontrollere at kateteret er riktig plassert.
- Vaginalvask med klorhexidin har ikke vist forebyggende effekt mot infeksjon.
- Kateter føres gjennom livmorhals forbi indre mormunn. Kan enklest gjøres ved hjelp av selvholdende spekel og korntang. Ikke grip livmorhals med kuletang pga. risiko for rift og blødning.
- Fyll ballongen med 80 ml NaCl. Dersom ballongen ligger i livmorhalsen, vil kvinnen ofte få smerter umiddelbart. Trekk da ut noe av væsken og skyv kateteret litt lenger inn. Cooks vaginal (ytre) ballong ligger oftest i livmorhalsen ved lang, kollagenrik cervix. Det kan være smertefullt for kvinnen ved max. volum i ytre ballong, man kan imidlertid forsøke å fylle på mer væske etter noen timer, opp til 80 ml.
- Fest kateteret uten stramming med tape til kvinnens lår ved bruk av Foleykateter [39].
- Kateteret kan ligge i 12- 36 timer (12- 24 timer ved vannavgang uten infeksjonstegn) [40], [41].
Komplikasjoner ved kateterinduksjon og PROM
En svensk[42] (2008) og en amerikansk studie (2017)[43] indikerer ikke større risiko for amnionitt ved kateterigangsettinger når PROM foreligger. En retrospektiv finsk studie (2020) fant heller ikke økt forekomst av infeksjon hos mor eller foster ved bruk av kateterinduksjon ved PROM til termin sammenlignet med kvinner uten PROM.[44] Mer kortvarig kateterigangsetting anbefales dersom det foreligger PROM (12-24 timer) (forslag). Det er ikke gjort studier med kateterinduksjon og pPROM men det kan vurderes kateterinduksjon dersom ingen infeksjonstegn og umoden livmorhals.
Poliklinisk fødselsinduksjon med ballongkateter
Dersom kvinnen eller fosteret ikke trenger overvåking, og svangerskapet ikke har tegn til patologi, kan poliklinisk induksjon vurderes. Eksempler på lav-risiko svangerskap: svangerskapslengde 41+ uten annen patologi, intrahepatisk svangerskapskolestase, mild preeklampsi, kostregulert svangerskapsdiabetes, bekkenløsning. Kvinnen må få skriftlig informasjon om induksjonen. Kvinnen skal kunne komme til fødeavdelingen straks hun får rier. Kontaktinformasjon må stå tydelig på informasjonen, samt informasjon om når kvinnen skal kontakte fødeavdelingen (se vedlagt Pasientinformasjon).
Følgende muligheter foreligger etter ballonginnleggelse (12-36 timer)
- Ballongen faller ut. Vurder videre induksjon med amniotomi/oxytocin
- Kvinnen har fått rier og er i fødsel
- Fostervannet har avgått, ikke rier
- Igangsetting med prostaglandin eller oxytocin
- Ikke vannavgang eller rier
- Moden livmorhals → amniotomi
- Umoden livmorhals → videre modning med prostaglandin
3. Igangsetting med prostaglandin (I)[45]
Tablett (Cytotec® tabletter/Pfizer, Angusta® tabletter/Azanta AS)
Misoprostol er en syntetisk prostaglandin E1-analog som har tilsvarende virkningsmekanisme som dinoproston (Minprostin®, Pfizer) endocervical gel og (Prostin E2®, Orifarm) vaginaltablett. Misoprostol er mer effektiv til modning av livmorhals med hensyn til igangsetting av fødsel (I) og har mye kraftigere modningseffekt på livmorhals nærmere termin, sammenlignet med i tidlig graviditet og hos ikke-gravide.
Preparater:
- Angusta® 25 µg misoprostol tabletter til peroral bruk.
Dosering: 25 µg hver 2. time eller 50 µg hver 4. time iht. sykehusets rutiner, maks. døgndose 200 µg. Av kontraindikasjoner i Felleskatalogteksten, bør man merke følgende: Ved mistanke om/bevis på arrvev fra tidligere kirurgiske inngrep i uterus eller cervix, f.eks. keisersnitt. - Cytotec® er ikke registrert på indikasjonen modning av livmorhals/igangsetting av fødsel av Pfizer. I Norge brukes Cytotec® ved flere sykehus i stedet for andre prostaglandiner. Misoprostolkapsler på ca. 25 µg lages fra Cytotec® ved flere større norske sykehusapotek. Dosering: Misoprostol (Cytotec®) 25 µg i bakre fornix. Samme dose kan gjentas hver 3. - 6. time dersom regelmessig riaktivitet ikke er etablert (I). Ved manglende respons og umoden cervix hos førstegangsfødende økes dosen vaginal misoprostol til 50 µg etter to doser. Maks døgndose vaginal misoprostol dosering 150 µg (forslag).
Man kan gi misoprostol mer enn ett døgn. Det er ingen kjent total maksdose.
Prostaglandiner og oxytocin til kvinner med tidligere keisersnitt er assosiert med økt risiko for uterusruptur. De bør derfor benyttes med varsomhet og under tett kontinuerlig fosterovervåkning. Man bør ha lavere terskel for å vurdere keisersnitt ved mistanke om misforhold, feilinnstilling eller protraherte forløp enn hos kvinner som ikke har tidligere arr i uterus.
Peroral eller vaginal dosering av misprostol?
Farmakokinetiske studier på kvinner i forbindelse med første trimester aborter viser at sublingual og peroral dosering av misoprostol fører raskere til uteruskontraksjoner enn vaginal misoprostol, men effekten er svakere enn ved vaginaldosering.[46] Misoprostol metaboliseres med en helt annen farmakokinetikk via peroral, sammenlignet med vaginal dosering. Dette betyr at 25 µg peroral misoprostol og 25 µg vaginal misoprostol ikke er ekvivalente. 25 µg vaginal misoprostol x 2 (50 µg) tilsvarer 6-9 tabletter 25 µg peroral misoprostol. Dette har også betydning for dosering og bruk av prostaglandiner hos overvektige. Det er ikke gjort noen farmakokinetiske studier på bruken av prostaglandiner på kvinner som får fødselen sin indusert.[47] Det er grunn til å anta at misoprostol metaboliseres dårligere ved peroral dosering hos overvektige kvinner, enn vaginal dosering, pga. økt distribusjonsvolum og økt first-pass effekt via gastrointesintal-systemet. Angusta® er ikke godkjent til vaginal dosering.
Vaginal absorbsjon av misoprostol reduseres av blod[48] og endring av vaginal flora.[49] For optimal dosering av vaginal misoprostol vil man få største opptak ved vaginal applikasjon av Cytotec® kapsler gjennomført med kvinnen i benholdere, med plassering av vaginal Cytotec® kapsel i bakre fornix, etter at blod og slim fra vagina er tørket vekk.
”UpToDate” (mai 2019)[50] anbefaler vaginal misoprostol som metode (kontraindisert ved tidligere keisersnitt). WHO1 anbefaler peroral lavdose misoprostol (20-25 μg hver 2. time) da dette anses tryggere og mer effektivt enn vaginal misoprostol (kontraindisert ved tidligere keisersnitt (III). Vaginal misoprostol i doser over 25 μg er mer effektiv enn andre metoder for igangsetting av fødsel, men er forbundet med større risiko for hyperstimulering av uterus (I). Ved manglende respons og umoden cervix hos førstegangsfødende økes dosen vaginal misoprostol til 50 µg etter to doser. Mak døgndose 150 µg vaginal misoprostol. Det er økt risiko for hyperstimulering/riestorm med 50 µg dose vaginal misoprostol.
Poliklinisk induksjon med oral misoprostol for lavrisiko svangerskap
Poliklinisk induksjon med oral misoprostol anses som et alternativ til innleggelse for kvinner med lavrisiko svangerskap og der det anses trygt at kvinnen er hjemme inntil riestart[51]. Det bør foreligge en skriftlig retningslinje med klare kriterier samt prosedyrer for oppfølging hjemme. Kvinnen bør få muntlig og skriftlig informasjon.
Propess® vaginalinnlegg (Dinoprostone 10mg).
Vaginalinnlegget frigir 0,3 mg PGE2/time over 24 timer.
Godkjent til av cervixmodning hos pasienter ved termin (fra 37 fullgåtte svangerskapsuker). Skal brukes alene, uten samtidig bruk av andre midler til fødselsinduksjon (f.eks. kateter, andre prostaglandiner eller oxytocin). Kontraindisert ved tidligere keisersnitt eller myomektomi. Kan brukes ved PROM.
Intravaginal applikasjon av dinoprostone (PGE2) tablett (Prostin E2® vaginaltablett Orifram, ikke registrert preparat)
I den norske induksjonsstudien (2018)[4] var induksjon med dinoprostone assosiert med høyere forekomst av forløsning med keisersnitt. Dette gjelder kun Robson 2.
Dosering: 1 tablett à 3 mg. Kan gjentas etter seks timer. Maks dose 9 mg/døgn.
Komplikasjoner
Hyperton riaktivitet (overstimulering) av uterus kan forekomme ved igangsetting med alle prostaglandiner. Prostaglandiner gitt ved moden livmorhals er forbundet med økt risiko for hyperstimulering (I). Uterusruptur kan forekomme. Ved tidligere keisersnitt eller tidligere operasjon på uterus bør kateter være første valg for igangsetting (III).
Andre alternativer
Amniotomi hvis mulig (livmorhals <2 cm), Bishops score fortrinnsvis >5 hos multipara, fortrinnsvis >7 hos nullipara. Hvis ingen riaktivitet etter en til tre timer, stimuleres med oksytocin intravenøst. Amniotomi eventuelt etterfulgt av oksytocin anbefales som første valg ved moden livmorhals (III).
Oksytocin intravenøst
Komplikasjoner
Amnionitt og hyperton riaktivitet kan forekomme ved amniotomi/oksytocinigangsetting. Bruk av oxytocin hos kvinner med tidligere keisersnitt er assosiert med økt risiko for uterusruptur. Medikamentet bør derfor benyttes med varsomhet og under CTG overvåkning og tilleggsmetoder. Man bør ha lavere terskel for å vurdere keisersnitt ved mistanke om misforhold, feilinnstilling eller protrahert forløp hos kvinner med arr i uterus.
Fosterovervåkning ved igangsetting (IV)
- CTG-registrering før modning/igangsetting, 20-30 minutter.
- Ved normal CTG-registrering hos inneliggende pasienter uten rier:
Vaginal misoprostol: CTG 20-30 minutter før hver ny vaginal kapsel (hver 4. – 6. time). Ny CTG-registrering ved endring i forløpet som begynnende riaktivitet, smerter eller vannavgang. CTG før leggetid dersom ingen rier.
Peroral misoprostol: CTG 20-30 minutter etter tre tabletter 25 µg peroral misoprostol eller ny CTG ved endring i forløpet som begynnende riaktivitet, smerter eller vannavgang. Ved fortsatt normal CTG registrering tas det ny CTG 20-30 minutter etter ytterligere tre doser peroral misoprostol, før leggetid. - Ny CTG-registrering ved endring i forløpet som begynnende riaktivitet, smerter eller vannavgang. Deretter intermitterende, evt. kontinuerlig overvåkning
Komplikasjoner
Hyperton riaktivitet (seks eller flere kontraksjoner per 10 minutter): Risiko 1-5 %.
Behandling
Seponere oxytocin, forsøke intrauterin resusitering med Atosiban (Tractocile®, Ferring Pharmaceuticals A/S) 7,5 mg/ml, 0,9 ml (hetteglass) = 6,75 mg i.v. over minst ett minutt. Kan gjentas dersom riestormen tar seg opp igjen.
Igangsetting ved senabort/intrauterin fosterdød [45]
Unngå vaginal dosering av Cytotec ved blødning og/eller infeksjonstegn.
Metode: Før svangerskapsuke 24: (sterk anbefaling) 200 mg mifepriston (Mifegyn®, Mifepristone) per os. 36-48 timer senere: 800 µg misoprostol vaginalt. Dette er 4 stk. 200 µg tabletter misoprostol (Cytotec®, Pfizer) (ikke det samme som 25 µg kapsler misoprostol Cytotec® til fødselsigangsetting). Om kvinnen ikke får rier skal det etter 3 timer gis 400 µg misoprostol (dvs. 2 stk. 200 µg tabletter Cytotec®) peroralt eller sublingualt og hver tredje time deretter til hun får rier.
Ved svangerskapsuke 24 til uke 26: (sterk anbefaling) 200 mg mifepriston (Mifegyn®, Mifepristone) per os. 36-48 timer senere: 100 µg misoprostol vaginalt. Om kvinnen ikke får rier gis det etter tre timer 100 µg misoprostol peroralt eller sublingualt og hver tredje time videre, maksimalt fire doser. Dersom kvinnen fremdeles ikke får rier må det vurderes om forholdene ligger til rette for amniotomi og stimulering med oksytocin. Oksytocin gis vanligvis i dobbel styrke. Amniotomi vurderes individuelt - tilbakeholdenhet ved umoden livmorhals og forventet lang igangsettingstid.
Svangerskapsuke 27-43: (forslag) 200 mg mifepriston (Mifegyn®, Mifepristone) per os. 36-48 timer senere: Vurdere modenhetsgraden av livmorhals. 25 µg misoprostol vaginalt hver 6. time eller 25 µg misoprostol per oralt hver 2. time. Etter to doser kan man doble dosen dersom ingen rier. Vurdering etter seks doser dersom ingen effekt. Kan vurdere vanlig igangsettingsprosedyre med ballongkateter, misoprostol (25 µg kapsler hver 6. time), eller amniotomi.
Referanser
[1] World Health Organization (2011) WHO recommendations for induction of labour. https://apps.who.int/iris/bitstream/handle/10665/44531/9789241501156_eng.pdf?sequence=1 (lest 2019.05.26)
[2] Sennström M, Ekman G, Westergren-Thorsson GW, Malmström A, Byström B, Endrésen U, Mlambo N, Norman M, Ståbi B, Brauner A. Human cervical ripening, an inflammatory process mediated by cytokines. Mol Hum Reprod 2000; 6: 375–381.
[3] http://statistikkbank.fhi.no/mfr/ (lest 2020.11.25).
[4] Sørbye IK, Oppegaard KS, Weeks A, Marsdal K, Jacobsen AF. Induction of labor and nulliparity; A nationwide clinical practice pilot evaluation. AOGS 2020: 99; 1700-1709. https://doi.org/10.1111/aogs.13948
[5] Dögl M, Vanky E, Heimstad R. Changes in induction methods have not influenced cesarean section rates amoung women with induced labor. AOGS 2016: 95; 112-115.
[6] https://www.helsedirektoratet.no/statistikk/statistikk/kvalitetsindikatorer/graviditet-og-fodsel/igangsetting-av-fødsel (lest 2019.05.26).
[7] Joshua P. Vogel JP., Souza JP. and Gülmezoglu AM. Patterns and Outcomes of Induction of Labour in Africa and Asia: A Secondary Analysis of the WHO Global Survey on Maternal and Neonatal Health. PLoS One. 2013; 8(6): e65612.
[8] Fondazione Confalonieri Ragonese. Induzione al travaglio di parto: linee guida SIGO, AOGOI, AGUI. [Induction of labour: guidelines SIGO, AOGOI, AGUI] (in Italian). 2016. Available online at: https://www.sigo.it/wp-content/uploads/2016/03/Induzione-al-Travaglio-di-Parto.pdf (lest 2019.09.08)
[9] Middleton P, Shepherd E, Crowther CA. Induction of labour in women with normal pregnancies at or beyond term. Cochrane Review 2018. https://www.cochrane.org/CD004945/PREG_induction-labour-women-normal-pregnancies-or-beyond-term (lest 2019.05.31)
[10] Rydal E. Declercq E, Juhl M, Maimburg RD. Routine induction in late-term pregnancies: follow-up of a Danish induction of labour paradigm. BMJ Open 2019;9:e032815. doi:10.1136/bmjopen-2019-032815.
[11] Koopmans CM, Bijlenga D, Groen H, et al. Induction of labour versus expectant monitoring for gestational hypertension or mild pre-eclampsia after 36 weeks' gestation (HYPITAT): a multicentre, open-label randomised controlled trial. Lancet 2009; 374(9694): 979-988.
[12] Berger H and Melamed N. Timing of delivery in women with diabetes in pregnancy. Obstetric Medicine 2014: 7; 8-16.
[13] Diabetes in pregnancy: management from preconception to the postnatal period. NICE Guidelines 2015. https://www.nice.org.uk/guidance/ng3/resources/diabetes-in-pregnancy-management-from-preconception-to-the-postnatal-period-pdf-51038446021 (lest 2019.05.31)
[14] Oddie S, Embleton ND. Risk factors for early onset neonatal group B streptococcal sepsis: case-control study. BMJ. 2002; 325: 308.
[15] Middleton P, Shepherd E, Flenady V, McBain RD, Crowther CA. Is it better for a baby to be born immediately or to wait for labour to start spontaneously when waters break at or after 37 weeks? Cochrane Review 2017. https://www.cochrane.org/CD005302/PREG_it-better-baby-be-born-immediately-or-wait-labour-start-spontaneously-when-waters-break-or-after-37 (lest 2019.05.31)
[16] BMC Pregnancy Childbirth. 2015 Jun 16;15:136. doi: 10.1186/s12884-015-0566-4. Induction of twin pregnancy and the risk of caesarean delivery: a cohort study. Jonsson M.
[17] Dodd JM, Deussen AR, Grivell RM, Crowther CA. Elective birth of women with an uncomplicated twin pregnancy from 37 weeks' gestation, Cochrane Review 2014. https://www.cochrane.org/CD003582/PREG_elective-birth-of-women-with-an-uncomplicated-twin-pregnancy-from-37-weeks-gestation (lest 2019.05.31)
[18] Ovadia C, Seed PT, Sklavounos A, et al. Association of adverse perinatal outcomes of intrahepatic cholestasis of pregnancy with biochemical markers: results of aggregate and individual patient data meta-analyses. Lancet 2019; published online Feb 14. http://dx.doi.org/10.1016/S0140-6736(18)31877-4.
[19] WHO recommendation on induction of labour in women with gestational diabetes. 2011. https://extranet.who.int/rhl/topics/preconception-pregnancy-childbirth-and-postpartum-care/induction-labour/who-recommendation-induction-labour-women-gestational-diabetes (lest 2019.05.31).
[20] Bond DM, Gordon A, Hyett J, de Vries B, Carberry AE, Morris J. Early birth compared with waiting for birth in babies who are thought to be coping poorly towards the end of pregnancy, Cochrane Review. 2015. https://www.cochrane.org/CD009433/PREG_early-birth-compared-waiting-birth-babies-who-are-thought-be-coping-poorly-towards-end-pregnancy (lest 2019.05.31).
[21] Boers KE et al. Induction versus expectant monitoring for intrauterine growth restriction at term: randomised equivalence trial (DIGITAT). BMJ 2010; 341: c 7087.
[22] Boulvain M, Senat MV, Perrotin F, Winer N, Beucher G, Subtil D et al. Induction of labour versus expectant management for large-for-date fetuses: a randomised controlled trial. Lancet. 2015: 385: 2600-2605.
[23] Moldéus K, Cheng YW, Wikström AK, Stephansson O. Induction of labor versus expectant management of large-for-gestational-age infants in nulliparous women. PLoS One. 2017: 20; 12(7):e0180748.
[24] Magro-Malosso ER, Saccone G, Chen M, Navathe R, Di Tommaso M, Berghella V. Induction of labour for suspected macrosomia at term in non-diabetic women: a systematic reviewand meta-analysis of randomized controlled trials. BJOG. 2017; 124: 414-421.
[25] Dögl M, Romundstad P, Berntzen LD, Fremgaarden OC, Kirial K, Kjøllesdal AM, et al. Elective induction of labor: A prospective observational study. PLoS ONE 2018. 13(11): e0208098. https://doi.org/10.1371/journal.pone.0208098
[26] AA Boatin, F Cullinane, MR Torloni and AP Betrán. Audit and feedback using the Robson classification to reduce caesarean section rates: a systematic review. BJOG. 2018 Jan; 125: 36–42. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5763379/ (lest 2019.09.08).
[27] Vogel JP, et al. WHO Multi-Country Survey on Maternal and Newborn Health Research Network. Use of the Robson classification to assess caesarean section trends in 21 countries: a secondary analysis of two WHO multicountry surveys. Lancet Glob Health. 2015;3(5):e260-270.
[28] Ehrenthal DB, Jiang X, Strobino DM. Labor induction and the risk of a cesarean delivery among nulliparous women at term. Obstet Gynecol. 2010;116(1):35-42. Epub 2010/06/23.
[29] Le Ray C, Carayol M, Breart G, Gof net F. Elective induction of labor: failure to follow guidelines and risk of cesarean delivery. Acta Obstet Gynecol Scand. 2007;86(6):657-665. Epub 2007/05/24.
[30] Luthy DA, Malmgren JA, Zingheim RW. Cesarean delivery after elective induction in nulliparous women: the physician effect. Am J Obstet Gynecol. 2004;191(5):1511-1515.
[31] VA Danilack, DD Dore, EW Triche, JH Muri, MG Phipps, DA Savitza. The effect of labour induction on the risk of caesarean delivery: using propensity scores to control confounding by indication. BJOG. 2016; 123: 1521-1529.
[32] Mishanina E, Rogozinska E, Thatthi T, Uddin-Khan R, Khan KS, Meads C. Use of labour induction and risk of cesarean delivery: a systematic review and meta-analysis. CMAJ. 2014; 186: 665-673.
[33] West HM, Jozwiak M, Dodd JM. Methods of term labour induction for women with a previous caesarean section. Cochrane Database Syst Rev. 2017; 6: CD009792.
[34] Dögl M, Skogvoll E, Heimstad R. Cervical insulin-like growth factor binding protein-1 (IGFBP-1) to predict spontaneous onset of labor and induction to delivery interval in post-term pregnancy. Acta Obstet Gynecol Scand. 2011; 90(1): 57-62.
[35] Bishop E. Pelvic Scoring for elective induction. Obstet Gynecol 1964. 24; 2: 266-268.
[36] Laughon SK, Zhang J, Troendle J, Sun L, Reddy UM. Using a simplified Bishop score to predict vaginal delivery. Obstet Gynecol. 2011; 117: 805-811.
[37] Jozwiak M, Bloemenkamp KWM, Kelly AJ, Mol BWJ, Irion O, Boulvain M Mechanical methods for induction of labour. Cochrane Review 2012. https://www.cochrane.org/CD001233/PREG_mechanical-methods-for-induction-of-labour (lest 2019.05.31)
[38] Jozwiak M, Bloemenkamp KWM, Kelly AJ, Mol BWJ, Irion O, Boulvain M. Mechanical methods for induction of labour. Cochrane Database of Systematic Reviews 2012, Issue 3. Art. No.: CD001233. DOI: 10.1002/14651858.CD001233.pub2
[39] Schoen CN, Saccone G, Berghella V, Baker EG. Traction versus no traction in Foley catheter use for induction of labor: a systematic review and meta-analysis of randomized trials. Am J Obstet Gynecol MFM. 2022 Mar 4:100610. doi: 10.1016/j.ajogmf.2022.100610. Epub ahead of print. PMID: 35257939.
[40] Gomez Slagle HB, Fonge YN, Caplan R, Pfeuti CK, Sciscione AC, Hoffman MK. Early vs expectant artificial rupture of membranes following Foley catheter ripening: a randomized controlled trial. Am J Obstet Gynecol. 2021 Dec 27:S0002-9378(21)02628-4. doi: 10.1016/j.ajog.2021.11.1368. Epub ahead of print. PMID: 35135684.
[41] Lassey SC, Haber HR, Kanbergs A, Robinson JN, Little SE. Six versus twelve hours of single-balloon catheter placement with oxytocin administration for labor induction: a randomized controlled trial. Am J Obstet Gynecol. 2021 Jun;224(6):611.e1-611.e8. doi: 10.1016/j.ajog.2021.03.021. Epub 2021 Mar 23. PMID: 33771496.
[42] Prager M, Eneroth-Grimfors E, Edlund M, Marions L. A randomised controlled trial of intravaginal dinoprostone, intravaginal misoprostol and transcervical balloon catheter for labour induction. BJOG. 2008; 115:1443-1450.
[43] Amorosa JMH, Stone J, Factor SH, Booker W, Newland M, Bianco A. A randomized trial of Foley Bulb for Labor Induction in Premature Rupture of Membranes in Nulliparas (FLIP). Am J Obstet Gynecol. 2017; 217: 360.e1-360.e7.
[44] Kruit H, Tolvanen J, Eriksson J, Place K, Nupponen I, Rahkonen L. Balloon catheter use for cervical ripening in women with term pre-labor rupture of membranes: A 5-year cohort study. Acta Obstet Gynecol Scand. 2020 Apr 3. doi: 10.1111/aogs.13856.
[45] https://www.figo.org/sites/default/files/uploads/project-publications/Miso/FIGO_Dosage_Chart%20EN_0.pdf (lest 2019.05.31)
[46] Aronsson A, Bygdeman M, Gemzell-Danielsson K. Hum Reprod. 2004; 19: 81-4. Effects of misoprostol on uterine contractility following different routes of administration.
[47] Tang O.S., Gemzell-Danielsson K, Ho, P.C. Misprostol: Pharmacokintetic profiles, effects on the uterus and side-effects. Int J Gynecol Obstet 2007; 99: 160-167.
[48] Tang OS, Schweer H, Lee SW, Ho PC. Pharmacokinetics of repeated doses of misoprostol. Hum Reprod. 2009; 24: 1862-1869.
[49] Sioutas A. Sandström C. Fiala B. Watzer H. Schweer K. Gemzell-Danielsson. Effect of bacterial vaginosis on the pharmacokinetics of misoprostol in early pregnancy Human Reproduction 2012; 27: 388–393.
[50] https://www.uptodate.com/contents/techniques-for-ripening-the-unfavorable-cervix-prior-to-induction (lest 2019.05.27)
[51] Helmig RB, Hvidman LE. An audit of oral administration of Angusta® (misoprostol) 25 µg for induction of labor in 976 consecutive women with a singleton pregnancy in a university hospital in Denmark. Acta Obstet Gynecol Scand. 2020 Oct;99(10):1396-1402. doi: 10.1111/aogs.13876. Epub 2020 May 19. PMID: 32311758.