Anbefalinger
- Vi anbefaler at serum gallesyrer, levertransaminaser (ASAT/ALAT), gamma-GT og bilirubin kontrolleres hos alle gravide som har kløe uten hudutslett.[1] Forhøyet nivå av serum gallesyrer (> 10 μmol /L) er diagnostisk for intrahepatisk svangerskapskolestase (ICP). (I) Ved sterkt forhøyede levertransaminaser og/eller gulsott bør INR kontrolleres.[2]
- Vi anbefaler behandling med ursodeoksykolsyre ved innsettende ICP tidlig i svangerskapet, eller ved sterk kløe. Dersom 1g/dag ikke er tilstrekkelig for å redusere kløe og senke gallesyrenivået til < 100 µmol/L, kan dosen økes til 1,5 – 2g/dag (IV).
- Vi anbefaler at alle gravide med ICP får kontrollert sine biokjemiske markører ukentlig (III).
- Vi anbefaler at kvinner med ICP med gallesyrenivå > 100 µmol/L, til tross for behandling, forløses svangerskapsuke 34-35 (II).
- Vi anbefaler at kvinner med ICP med gallesyrenivå < 100 µmol/L forløses svangerskapsuke 38+0 – 38+6 (II).
Søkestrategi
Pyramidesøk McMaster PLUS (via Helsebiblioteket.no), UpToDate, PubMed, Cochrane Database, American College of Obstetricians and Gynecologists (ACOG), Royal College of Obstetricians and Gynecologists (RCOG), World Health Organization (WHO). Søkeord “obstetric cholestasis”, “cholestasis in pregnancy”, “systematic review”, and “meta-analysis”.
Søkeord for app-versjonen
kløe, kolestase, intrahepatisk svangerskapskolestase, svangerskapskløe
Definisjon
Forhøyede gallesyrer og/eller leverfunksjonsprøver ledsaget av kløe uten utslett, spesielt i hender og under fotsålene, som debuterer i svangerskap. Forhøyet nivå av serum gallesyrer (> 10 µmol/L) er diagnostisk for intrahepatisk svangerskapskolestase (ICP)(I)[3]. Kløen er ofte intens og kan debutere før biokjemiske avvik påvises. I 80% av tilfellene, oppstår ICP etter svangerskapsuke 24 men høye verdier av gallesyrenivåer har vært påvist også i første trimester.
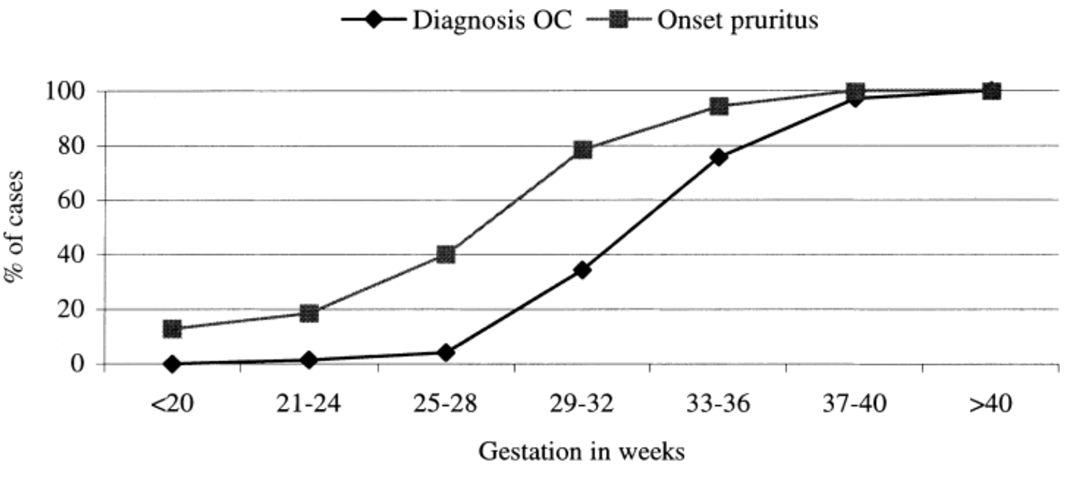 Fra Kenyon AP. et al. Obstetric cholestasis, outcome with active management: a series of 70 cases. BJOG 2002; 109: 282-8.
Fra Kenyon AP. et al. Obstetric cholestasis, outcome with active management: a series of 70 cases. BJOG 2002; 109: 282-8.
Det er viktig å skille mellom obstetrisk kolestase og andre årsaker til kløe. Uspesifikk svangerskapskløe (pruritus gravidarum) forekommer hyppig i svangerskap (20-25 % av gravide), dessuten finnes graviditetsspesifikke hudsykdommer og andre hudsykdommer.
Epidemiologi
Intrahepatisk svangerskapskolestase oppstår i 0,2‐2 % av svangerskap.[4] Forekomsten varierer i forskjellige land og mellom etniske befolkningsgrupper. Kvinner fra Chile, Peru og Pakistan synes å ha høyere risiko (opptil 28% hos araucanianindianerne i Chile).[5] Det er ingen studier som viser forekomsten i Norge men en studie fra 2018 fra 21 norske fødeinstitusjoner viste at 2.4% av alle igangsettelser av fødsel hadde intrahepatisk svangerskapskolestase som indikasjon. De fleste kvinner med ICP er asymptomatiske når de ikke er gravide men 20% opplever kløe i lutealfasen av menstruasjonssyklus, eller ved bruk av østrogenholdig prevensjon.[6]
Komplikasjoner
Kohortundersøkelser fra Sverige[7] og Storbritannia[8] har vist at svangerskap hvor maternell serum gallesyrenivå er ≥ 40 µmol/L, er assosiert med økt forekomst av preterm fødsel (både spontan og iatrogen), mekonium i fostervannet og føtal asfyksi.
Intrauterin fosterdød er en fryktet komplikasjon (II). En stor metaanalyse (2019) av individuell pasientdata fra 56 studier, der 5269 pasienter med ICP ble inkludert, viste at risikoen for intrauterin fosterdød er signifikant økt når maternelle serum-gallesyrer nivå er ≥ 100 μmol/L eller høyere, sammenlignet med risikoen for intrauterin fosterdød blant kvinner uten intrahepatisk kolestase.1 Studien viste en prevalens av intrauterin fosterdød i svangerskap med ett foster på:
- 3/2310 eller 0.13% (95% CI 0.02–0.38) ved intrahepatisk kolestase med total serum gallesyrer < 40 μmol/L.
- 4/1412 eller 0.28% (95% 0.08–0.72) ved total serum gallesyrer 40-99 μmol/L og
- 18/514 eller 3.44% (95% CI 2.05–5.37) ved total serum gallesyrer ≥ 100 μmol/L.
Patofysiologi
Den nøyaktige årsaken til svangerskapskolestase er ikke fastlagt. Genetisk faktor anslås som årsak hos 16-35% (dominant arvelig, relativ risiko på 24 for ICP hos søstre, relativ risiko på 30 for ICP hos døtre). Forhøyede nivåer av kjønnshormoner i serum antas også å spille en sentral rolle. Tvillinggravide har opptil fem ganger økt risiko for ICP [9]. Kvinner som tidligere har hatt svangerskapskolestase har dessuten økt risiko for å få kløe og leverfunksjonsforstyrrelse ved inntak av p-piller.
Man tror at fosterkomplikasjonene kan skyldes økt nivå av serumgallesyrer hos fosteret (I). Mekoniumavgang kan ha sammenheng med at gallesyrene stimulerer tarmmotilitet. Hypotesen i forhold til prematur fødsel er at gallesyrene kan føre til økt prostaglandinfrigjøring og prostaglandinsyntese.[10] Hypotesen i forhold til fosterdød er at gallesyrene kan ha en direkte toksisk effekt på fosterets myocard.[11]
Symptomer
Generelt utbredt kløe uten utslett, spesielt i hender og under fotsåler. Kløen er mest uttalt om natten. Tilstanden er vanligst i 3. trimester. Kløen kan debutere før biokjemisk avvik. Det er ikke sammenheng mellom gallesyrenivået og kløeintensiteten.
Sekundære plager: tretthet, vekttap, epigastriesmerter, mørk urin, lys/hvit avføring, gallesten.
Differensialdiagnoser
Gallesten (ved tvil henvises til ultralyd lever/galleveier), preeklampsi/HELLP, akutt fettlever i svangerskap, virusinfeksjon.
Funn
- Økte gallesyrer (normalverdi <6 µmol/L). Referanseområdet er for fastende prøve. Dersom ikke-fastende prøve tas kan nivået være lett økt, i forhold til normalverdien. Ikke-fastende verdier vil kunne være tilstrekkelig for å påvise en eventuell betydelig stigning, som er vanlig ved tilstanden.[12]
Ved typisk kløe og normal verdi bør man vurdere å repetere prøvetaking etter en uke. - Moderat økte transaminaser (mindre enn tre ganger øvre grense for normalverdi) og gamma‐GT.
Overvåkning i svangerskapet
Vi anbefaler at alle gravide med ICP får kontrollert sine biokjemiske markører ukentlig (III). Dette kan gjerne gjøres hos fastlege. Ved sterkt forhøyede levertransaminaser og/eller gulsott bør INR kontrolleres. Ultralydundersøkelse og CTG-registrering kan ikke predikere intrauterin fosterdød ved svangerskapskolestase. Preterm fødsel er assosiert med både kortsiktige komplikasjoner neonatalt, og langsiktige komplikasjoner.[13],[14]
Vi anbefaler at kvinner med ICP med gallesyrenivå > 100 µmol/L, til tross for behandling, forløses svangerskapsuke 34-35 (II).
Vi anbefaler at kvinner med ICP med gallesyrenivå til < 100 µmol/L forløses svangerskapsuke 38+0 – 38+6. Igangsettelse av fødsel ser ut til å være en gunstig forløsningsmetode (IV). [15]
Medikamentell behandling
- Ursodeoksykolsyre (III). Det er en hydrofil gallesyre som erstatter den endogene gallesyren. Den reduserer gallesyrenivået reduseres og kan bedre kløen.[16] Vurderes til pasienter med symptomer tidlig i graviditeten eller ved uttalte plager. Preparat: ursodeoksykolsyre (Ursofalk®) 250 mg tabletter. Dosering 1 gram daglig i en dose. Pasienten må betale selv, hvit resept.
- Vitamin K (IV). Dersom det er påvist høy INR, bør Vitamin K gis i graviditeten, 10 mg daglig, fytometadion (Konakion Novum®) eller Vitacon® tabl. a 10 mg. (Fås på registreringsfritak, skriv vanlig hvit resept). Ved høy INR anbefales Vitamin K til mor ved fødselen (IV). 10 mg fytometadion (Konakion Novum® 10 mg/ml) iv, dvs. 1 ml, under fødsel eller rett før keisersnitt.
- Antihistaminer (IV). Forsøksvis antihistaminer som dekslorfeniram (Polaramin®), maks 12 mg/døgn. Kan lindre kløe og hjelpe ved søvnvansker. Cetirizindihydroklorid (Zyrtec®), 10 mg/døgn gir mindre sedasjon men kan lindre kløe.
- Rifampicin (IV). Ved alvorlige tilfeller av ICP kan behandling med Rifampicin vurderes.[17] Rifampicin legges til behandling med ursodeoksykolsyre og virker synergistisk med ursodeoksykolsyre ved å øke galleekskresjonen fra hepatocyttene i større grad enn ved ursodeoksykolsyre alene. Dosering Rifampicin 100 mg x 2 som kan økes til 200 mg x 2. Omtrent 50% har effekt på kløe og reduksjon av gallesyrer. Rifampicin gir leveraffeksjon hos 20–30% og leverfunksjonsprøver må kontrolleres under behandlingen. Rifampicin må seponeres ved signifikante kliniske endringer i leverfunksjonen. Trombocytopeni, purpura, hemolytisk anemi, dyspné og astmalignende anfall, sjokk og nyresvikt kan også forekomme under behandling med rifampicin. Rifampicin gitt i svangerskapets siste uker kan forårsake postnatal blødning hos mor og spedbarn, og behandling med vitamin K kan være indisert (se avsnittet Vitamin K).
- Plasmautskifting (IV). Plasmautskifting (plasmaferese) er beskrevet. Formålet er da å kvitte seg med kløefremkallende metabolitter og effekten varer i noen dager. Plasmautskiftning kan være aktuelt for å utsette forløsning til uke 34.[18]
Postpartum
Ursodeoksykolsyre seponeres etter fødsel. Kontroll av leverfunksjonsprøve hos fastlege etter 14 dager. Inntil 20% av disse pasientene får også kløe ved bruk av p‐piller. Kvinner som har hatt kolestase bør opplyses om at østrogenholdig prevensjon kan forårsake kløe. Noen har symptomer under eller etter menopause. HRT kan brukes da dette kun gir fysiologisk nivå av østrogen.
Gjentagelsesrisiko
Det er 90 % risiko for kolestase i neste svangerskap.
Pasientinformasjon
Referanser
[1] Ovadia C, Seed PT, Sklavounos A, et al. Association of adverse perinatal outcomes of intrahepatic cholestasis of pregnancy with biochemical markers: results of aggregate and individual patient data meta-analyses. Lancet 2019; published online Feb 14. http://dx.doi.org/10.1016/S0140-6736(18)31877-4.
[2] Nelson-Piercy C, Handbook of Obstetric Medicine, 5th Edition. CRC Press 2015, 212-217. ISBN-13: 978-1-4822-4193-8 (ebook-PDF).
[3] Lin J, Gu W, Hou Y. Diagnosis and prognosis of early-onset intrahepatic cholestasis of pregnancy: a prospective study. J Matern Fetal Neonatal Med 2017; published online Nov 7. DOI:10.1080/14767058.2017.1397124
[4] Williamson C, Geenes V. Intrahepatic cholestasis of pregnancy. Obstet Gynecol 2014; 124: 120–133.
[5] Geenes V, Williamson C. Intrahepatic cholestasis of pregnancy. World J Gastroenterol. 2009; 15: 2049–2066.
[6] Powrie R, Greene M, Camann W. de Swiet's Medical Disorders in Obstetric Practice, 5th Edition 2010, Wiley-Blackwell, 234-237.
[7] Glantz A, Marschall HU, Mattsson L.. Intrahepatic cholestasis of pregnancy: relationships between bile acid levels and fetal complication rates. Hepatology 2004; 40: 467–74.
[8] Geenes V, Chappell LC, Seed PT, Steer PJ, Knight M, Williamson C. Association of severe intrahepatic cholestasis of pregnancy with adverse pregnancy outcomes: a prospective population-based case-control study. Hepatology 2014; 59: 1482–1491.
[9] Gonzalez MC et al. Intrahepatic cholestasis of pregnancy in twin pregnancies. J Heptaol. 1989; 9: 84.
[10] Campos GA, Guerra FA, Israel EJ. Effects of cholic acid infusion in fetal lambs. Acta Obstet Gynecol Scand 1986; 65: 23–26.
[11] Gorelik J, Shevchuk A, de Swiet M, Lab M, Korchev Y, Williamson C. Comparison of the arrhythmogenic effects of tauro- and glycoconjugates of cholic acid in an in vitro study of rat cardiomyocytes. BJOG 2004; 111: 867-870.
[12] https://ehandboken.ous-hf.no/document/105061
[13] Chan E, Quigley MA. School performance at age 7 years in late preterm and early term birth: a cohort study. Arch Dis Child Fetal Neonatal Ed 2014; 99: F451–57.
[14] Rabie NZ, Bird TM, Magann EF, Hall RW, McKelvey SS. ADHD and developmental speech/language disorders in late preterm, early term and term infants. J Perinatol 2015; 35: 660–64.
[15] Friberg AK, Zingmark V, Lyndrup J. Early induction of labor in high-risk intrahepatic cholestasis of pregnancy: what are the costs? Arch Gynecol Obstet. 2016; 294 :709-714.
[16] Chappell LC, Gurung V, Seed PT, Chambers J, Williamson C, Thornton JG. Ursodeoxycholic acid versus placebo, and early term delivery versus expectant management, in women with intrahepatic cholestasis of pregnancy: semifactorial randomised clinical trial. BMJ 2012; 344: e3799–3799.
[17] Geenes V, Chambers J, Khurana R, Shermer EW, Sia W, Mandair D, Elias E, Marschall HU, Hague W, Williamson C. Rifampicin in the treatment of severe intrahepatic cholestasis of pregnancy. Eur J Obstet Gynecol Reprod Biol. 2015; 189: 59-63.
[18] Warren JE, Blaylock RC, Silver RM. Plasmapheresis for the treatment of intrahepatic cholestasis of pregnancy refractory to medical treatment. Am J Obstet Gynecol. 2005; 192: 2088-2089.