Anbefalinger
-
Vi anbefaler 5 IE oksytocin i.m. som primærprofylakse til alle ved normal fødsel (I)
-
Vi anbefaler 3 IE oksytocin langsomt i.v. ved keisersnitt, kan gjentas x 2 (I)
-
Vi anbefaler i.v. tranexamsyre (1 g i.v.) før hudincisjon ved keisersnitt hvor kvinnen har økt risiko for PPB (I).
-
Vi anbefaler i.v. tranexamsyre (1 g i.v.) tidlig ved pågående PPH (I)
-
Vi anbefaler oksytocindrypp 50 IE/500 ml NaCl/Ringer, 150 ml/time intravenøst ved PPH (I)
-
Vi anbefaler tidlig transfusjon ved alvorlig PPH (I)
-
Vi anbefaler behandling av antenatal anemi i svangerskapet (I)
Søkestrategi:
Pyramidesøk, Mc Master Plus, Cochrane Database, Royal College of Obstetricians & Gynaecologists (RCOG), Up To Date, PubMed.
Søkeord: postpartumblødning, blødning etter fødsel, atoni, etterbyrdsbløder, koagulasjonsforstyrrelser, DIC, transfusjon, fastsittende placenta, PPH, PPB.
Definisjoner
-
Tidlig postpartumblødning: >500 ml i løpet av de første 24 timer etter fødselen
-
Alvorlig postpartumblødning: >1000 ml blødning i løpet av første 24 timer etter fødsel
-
Livstruende blødning: > 40 % blodtap (ca. 2800 ml hos en kvinne på 70 kg)
-
Sen postpartumblødning: fra 24 timer til 12 uker postpartum
Epidemiologi
Postpartumblødning >500 ml: ca. 25 % av alle fødende.
Alvorlig postpartumblødning >1000 ml: ca. 5 % av alle fødende, >1500 ml: ca. 2,5 %.
Livstruende blødning: ca. 0,37 %.
Årsaker (1-3)
-
Tone: uterusatoni (60-80 %).
-
Trauma: rifter, hematom, uterusruptur, uterusinversjon (10%).
-
Tissue: placenta- og hinnerester (inkl. placenta accreta, percreta, increta) (10-30%).
-
Thrombin: koagulopati/Disseminert Intravaskulær Koagulasjon (DIC) (1%).
Husk at flere etiologiske faktorer kan opptre samtidig.
Sen postpartumblødning
Viktigste årsaker: Placenta- og hinnerester og/eller infeksjon i uterus.
Risikofaktorer (1, 3, 4)
-
Tidligere postpartumblødning
-
Lavtsittende placenta, placenta previa, invasiv placenta (accreta/increta/percreta),
-
Tidligere keisersnitt eller uteruskirurgi
-
Antepartum blødning
-
Langvarig fødsel, oksytocinstimulering, induksjon, operativ forløsning
-
Flerlingsvangerskap, polyhydramnion, stort barn (overdistendert livmor)
-
Maternell overvekt, høy alder, høy paritet
-
Myoma uteri
-
IVF/ICSI
-
Koagulasjonsforstyrrelser pga. alvorlig preeklampsi, HELLP, AFLP, placentaløsning.
-
Bruk av antikoagulantia
-
Intrauterin fosterdød, sepsis, embolier med gass/luft/fostervann
-
Blødningssykdommer: ITP, von Willebrands sykdom, Hemofili A og B, Trombasteni
Husk at risikofaktorene kan opptre både før og under fødsel og at de akkumuleres fortløpende. Man må derfor modifisere behandlingsplaner underveis når nye risikofaktorer tilkommer.
Diagnostikk av blodtap (5, 6)
Den visuelle estimeringen av blodtap under fødsel er unøyaktig. Det er derfor viktig å overvåke kliniske tegn og symptomer på stort blodtap i tillegg.
Det anbefales å måle det faktiske blodtapet, spesielt ved operative forløsninger, fremfor visuell estimering.
Gravide dekompenserer sent, dvs. at de kan ha store tap, og likevel presentere upåvirket fysiologi. Krever derfor tett og tverrfaglig oppfølging (obstetriker/anestesilege).
Samtidig hypotensjon og takykardi er ALLTID et alvorlig blødningstegn (i fravær av sepsis).
Behandling 7-13
Tabell 1. Medikamentell behandling i anbefalt rekkefølge
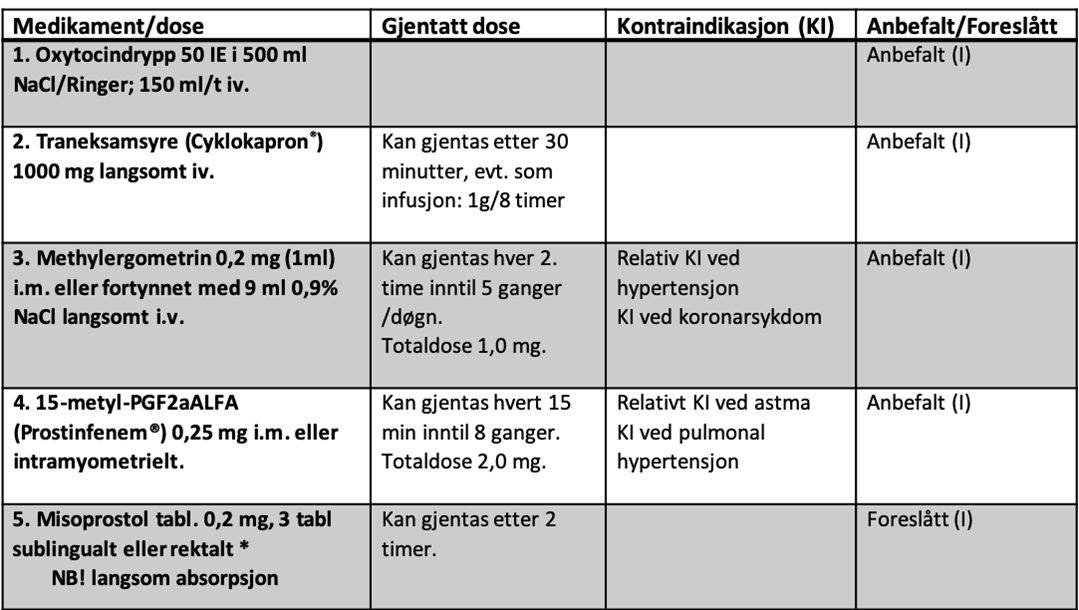
*Det er ikke påvist sikker tilleggseffekt av misoprostol i kombinasjon med andre uterotonika; anbefales derfor primært hvis andre uteruskontraherende medikamenter ikke er tilgjengelig (I). Rektal administrasjon har en farmakokinetisk profil som gir dårligere effekt enn sublingual administrasjon.
Vi anbefaler at fødestuer og operasjonsstuer har en” blødningsboks” med alle aktuelle medikamenter tilgjengelig.
Behandling ved pågående blødning:
Det er viktig at man bruker en kombinasjon av medikamenter, mekaniske og kirurgiske metoder for å stoppe blødningen, avhengig av årsaken til at kvinnen blør.
Vær raskt ute med kirurgiske intervensjoner dersom man ikke får stoppet blødningen med medikamenter.
Tiltak ved moderat blødning (500–1000 ml) uten kliniske tegn på sjokk
-
I.v. tilgang (2 grove kanyler)
-
Blodprøver: Hb, hct, trombocytter, typing og screening, evt. INR, fibrinogen, APTT
-
Estimert/målt blodtap, BT, respirasjonsfrekvens og puls overvåkes og registreres fortløpende
-
Start med oppvarmet i.v. væske (Ringer), inntil 1000 ml. Ved behov for større volum brukes blodprodukter dersom det er pågående blødning.
Videre tiltak ved større blødninger (>1000 ml), pågående blødning og/eller tegn på sjokk. Fortløpende vurdering av overflytning til operasjonsstuen.
-
Tilkall mer hjelp på fødestuen inkludert anestesilege
-
Legg pasienten flatt
-
O2 på maske
-
Start infusjon av varmede blodprodukter raskt
-
Bimanuell uteruskompresjon, inspeksjon og eksplorasjon, sutur av rifter (I)
-
Tøm urinblæren, evt. foleykateter
-
Forløsning av placenta på fødestuen hvis mulig (Credé)
-
Hypotermiprofylakse (oppvarmede i.v. væsker/varme tepper)
Intervensjoner på operasjonsstuen
-
Manuell uthenting av placenta/revisio (I). Ultralyd-kontroll kan være nyttig per- eller postoperativt ved mistanke om retinerte placentarester.
-
Sutur av dype vaginalrifter eller cervixrifter (II)
-
Bimanuell uteruskompresjon kontinuerlig evt. av assistent (fra starten) (I)
-
Uterustamponade med ballong (III)
-
Sutur av uterusruptur evt. placentasengen (III)
-
Kompresjonssutur (B-Lynch eller Hayman) ved uterusatoni (III)
-
Aortakompresjon (III)
-
Arteriell embolisering der det er tilgjengelig (III)
-
Aorta okklusjonsballong (REBOA) (III)
-
Devaskularisering av uterus: ligatur av aa. uterinae/aa. ovaricae (III)
-
Ligatur av aa. iliaca internae (evt. hjelp av erfaren kirurg)
-
Supravaginal uterusamputasjon/hysterektomi
-
«Pakking av buken» med kompresser hvis fortsatt pågående blødning og DIC (kontakt erfaren kirurg)
Rekkefølgen vil være avhengig av om dette er en vaginal fødsel eller keisersnitt.
I tillegg vil tilgjengelighet av intervensjonsradiolog og kompetanse på det enkelte sykehus være avgjørende for valg av intervensjon.
Transfusjon ved pågående alvorlig blødning (14-22)
Behandling av blodtap og væske startes parallelt med annen behandling (I-III).
Vi anbefaler
-
Ringer acetat. Unngå å gi mye krystalloider grunnet fare for fortynningskoagulopati (max. 1000 ml) før oppstart med blodprodukter.
-
Tidlig oppstart med transfusjon. Vurder både SAG og plasma (Octaplas®) initialt, alternativt massiv transfusjonspakke (5 SAG: 5 Plasma: 1 Trombocyttkons).
Det er mye som tyder på at plasmabehovet ikke er så stort i initialfasen av en PPB, gitt at det ikke foreligger koagulopati, som f.eks. ved placentaløsning/fostervannsemboli/preeklampsi m/koagulopati.
-
SAG og plasma (Octaplas®) ordineres i forholdet 1:1 så lenge blødningen pågår.
VE-POCT (Rotem®/TEG®) for fortløpende måling av koagulasjonsevnen er lovende, men fortsatt på forskningsstadiet.
-
Trombocytter bør transfunderes ved trombocytt-tall < 100x109/l (basert på lab.svar)
-
Fibrinogenkonsentrat anbefales (Riastap®): 4 g i.v. bør gis ved mistanke om tap av ett blodvolum evt. etter fibrinogen konsentrasjonsmåling. Et plasma-nivå ≥ 2,5 g/l bør tilstrebes.
-
Kalsiumtilskudd ved ionisert Ca2+< 1,2 mmol/l. (Kalsiumnivået er viktig for hemostasen og i-Ca må enten måles jevnlig, evt gis det 5-10 mmol CaCl2 per infundert massiv transfusjonspakke)
-
Desmopressin (Octostim®) er anbefalt ved hemofili/von Willebrands sykdom og evt. ved andre årsaker til dårlig fungerende trombocytter som ved bruk av acetylsalisylsyre.
Monitorér alle parametre på egnet overvåkningsskjema. Avvik skal utløse korreksjon.
-
Temp. overvåkes
-
Monitorering av resp.frekvens, puls og BT
-
Foleykateter med timediurese
-
Arteriekran
-
Dokumentér væskebalanse, estimert blødning, blodprodukter og utførte prosedyrer underveis
Behandlingsmål for resusitering (23)
-
Hb under pågående blødning ≥ 10 g/dl. Ved blødningskontroll ≥ 7 g/dl
-
INR <1,5
-
Fibrinogen ≥ 2,5 g/L
-
Trc ≥ 100x10^9/L
-
APTT <1,5 x normal blødningstid
-
Temp 37° C
-
Timediurese ≥ 0,5 ml/kg
-
PaO2 >12 kPa
-
Normalisering av laktat og BE
-
Ionisert Ca2+ ≥ 1,2 mmol/l
Vi anbefaler tromboseprofylakse innen 6 timer etter oppnådd hemostase og velkontrahert uterus ved alvorlig PPB. Disse kvinnene får en kraftig aktivering av koagulasjonssystemet etter blødningen, har økt risiko for infeksjon og er ofte immobilisert. Se for øvrig kapittel om trombose.
Profylakse i svangerskapet (1, 2, 24-26)
Antenatal anemi bør undersøkes og behandles adekvat i svangerskapet. Behandling reduserer forekomsten av maternell anemi etter fødsel, samt insidensen av lav fødselsvekt (I). Det er påvist en sammenheng mellom anemi i svangerskapet (Hb < 9 g/dl) og større blodtap under fødsel (III). I tillegg dekompenserer kvinner med anemi raskere ved en alvorlig blødning.
I.v. jern foreslås når p.o. jern ikke tolereres eller absorberes, ved dårlig compliance eller når kvinnen nærmer seg termin. Se for øvrig kapittel om anemi i svangerskapet.
Primærprofylakse (8, 27-30)
- Vi anbefaler 5 IE oksytocin i.m. ved normal fødsel (I)
a. Vi foreslår ytterligere 3 IE oksytocin langsomt i.v. ved økt risiko for PPB (II)
- Vi anbefaler 3 IE oksytocin langsomt i.v. ved keisersnitt, kan gjentas x 2 (I).
Oksytocin titreres én og én enhet intravenøst. Større bolusdoser til pasienter med kjent hjertesykdom og/eller hypovolemi kan gi sirkulasjonskollaps.
- Vi anbefaler i.v. tranexamsyre (1 g i.v.) før hudincisjon ved keisersnitt hvor kvinnen har økt risiko for PPB (I).
Aktiv håndtering av 3. stadium (27, 31-33)
Aktiv håndtering av 3. stadium reduserer risikoen for PPB, fastsittende placenta og anemi etter fødsel, og anbefales ved alle fødsler (I).
Vi anbefaler
- Primærprofylaktisk oksytocin (se over)
- Kontrollert drag i navlesnoren
Det er vist at sen avnavling (minst 2 min) er gunstig for barnet. Tidlig avnavling bør derfor ikke være en del av aktiv placentaforløsning (I).
Fastsittende placenta (34, 35)
Placenta bør være forløst innen 30 min. da risikoen for alvorlig blødning øker signifikant etter 30 min. Ved aktiv forløsning av placenta, får man forløst placenta i løpet av 30 min i 98% av tilfellene.
Konsekvenser for senere helse
- Uttalt anemi med kliniske symptomer
- Multiorgansvikt, spesielt nyresvikt
- Sheehan syndrom (hypofysesvikt)
- Komplikasjoner etter nødvendige kirurgiske inngrep
- Tap av fertilitet
- Sepsis
- Trombose
- Maternell død
Pasientinformasjon
Nøye informasjon og gjennomgang av forløpet i barseltiden er viktig. Etterkontroll med ny gjennomgang og vurdering av risikofaktorer ved alvorlig blødning.
Informeres om å gi beskjed til kontrollerende lege og jordmor ved neste svangerskap.
Innhent epikrise fra tidligere fødested ved mistanke om tidligere alvorlig PPB.
Gjentagelsesrisiko (1, 36)
Kvinner som har hatt en PPB har betydelig økt risiko for ny PPB i neste svangerskap. Pasienten bør derfor behandles som etterbyrdsbløder ved neste fødsel; aktiv forløsning av placenta og grov venekanyle.
Referanser
1. Nyflot LT, Sandven I, Stray-Pedersen B, Pettersen S, Al-Zirqi I, Rosenberg M, et al. Risk factors for severe postpartum hemorrhage: a case-control study. BMC Pregnancy Childbirth. 2017;17:17.
2. Oyelese Y, Ananth CV. Postpartum hemorrhage: epidemiology, risk factors, and causes. Clin Obstet Gynecol. 2010;53:147-56.
3. Al-Zirqi I, Vangen S, Forsen L, Stray-Pedersen B. Prevalence and risk factors of severe obstetric haemorrhage. BJOG. 2008;115:1265-72.
4. Nyflot LT, Sandven I, Oldereid NB, Stray-Pedersen B, Vangen S. Assisted reproductive technology and severe postpartum haemorrhage: a case-control study. BJOG. 2017;124:1198-205.
5. Glover P. Blood loss at delivery: how accurate is your estimation? Aust J Midwifery. 2003;16:21-4.
6. Rath WH. Postpartum hemorrhage--update on problems of definitions and diagnosis. Acta Obstet Gynecol Scand. 2011;90:421-8.
7. Mousa HA, Blum J, Abou El Senoun G, Shakur H, Alfirevic Z. Treatment for primary postpartum haemorrhage. Cochrane Database Syst Rev. 2014;2:CD003249.
8. Collaborators WT. Effect of early tranexamic acid administration on mortality, hysterectomy, and other morbidities in women with post-partum haemorrhage (WOMAN): an international, randomised, double-blind, placebo-controlled trial. Lancet. 2017;389:2105-16.
9. Doumouchtsis SK, Papageorghiou AT, Arulkumaran S. Systematic review of conservative management of postpartum hemorrhage: what to do when medical treatment fails. Obstet Gynecol Surv. 2007;62:540-7.
10. Hayman RG, Arulkumaran S, Steer PJ. Uterine compression sutures: surgical management of postpartum hemorrhage. Obstet Gynecol. 2002;99:502-6.
11. Pereira A, Nunes F, Pedroso S, Saraiva J, Retto H, Meirinho M. Compressive uterine sutures to treat postpartum bleeding secondary to uterine atony. Obstet Gynecol. 2005;106:569-72.
12. Gallos ID, Papadopoulou A, Man R, Athanasopoulos N, Tobias A, Price MJ, et al. Uterotonic agents for preventing postpartum haemorrhage: a network meta-analysis. Cochrane Database Syst Rev. 2018;12:CD011689.
13. Stensaeth KH, Sovik E, Haig IN, Skomedal E, Jorgensen A. Fluoroscopy-free Resuscitative Endovascular Balloon Occlusion of the Aorta (REBOA) for controlling life threatening postpartum hemorrhage. PloS one. 2017;12:e0174520.
14. Johansson PI, Stensballe J, Ostrowski SR. Current management of massive hemorrhage in trauma. Scand J Trauma Resusc Emerg Med. 2012;20:47.
15. Gonzalez EA, Moore FA, Holcomb JB, Miller CC, Kozar RA, Todd SR, et al. Fresh frozen plasma should be given earlier to patients requiring massive transfusion. J Trauma. 2007;62:112-9.
16. Padmanabhan A, Schwartz J, Spitalnik SL. Transfusion therapy in postpartum hemorrhage. Semin Perinatol. 2009;33:124-7.
17. Holcomb JB, del Junco DJ, Fox EE, Wade CE, Cohen MJ, Schreiber MA, et al. The prospective, observational, multicenter, major trauma transfusion (PROMMTT) study: comparative effectiveness of a time-varying treatment with competing risks. JAMA Surg. 2013;148:127-36.
18. Charbit B, Mandelbrot L, Samain E, Baron G, Haddaoui B, Keita H, et al. The decrease of fibrinogen is an early predictor of the severity of postpartum hemorrhage. J Thromb Haemost. 2007;5:266-73.
19. Cortet M, Deneux-Tharaux C, Dupont C, Colin C, Rudigoz RC, Bouvier-Colle MH, et al. Association between fibrinogen level and severity of postpartum haemorrhage: secondary analysis of a prospective trial. Br J Anaesth. 2012;108:984-9.
20. Hagemo JS, Stanworth S, Juffermans NP, Brohi K, Cohen M, Johansson PI, et al. Prevalence, predictors and outcome of hypofibrinogenaemia in trauma: a multicentre observational study. Crit Care. 2014;18:R52.
21. Collins PW, Cannings-John R, Bruynseels D, Mallaiah S, Dick J, Elton C, et al. Viscoelastometric-guided early fibrinogen concentrate replacement during postpartum haemorrhage: OBS2, a double-blind randomized controlled trial. Br J Anaesth. 2017;119:411-21.
22. Svenska sällskapet for trombos och hemostas (SSTH). Hemostas vid allvarliga blødningar 2017.https://www.ssth.se/wp-content/uploads/2017/04/vphemostas160330.pdf
23. Skaga NO HA, Meidell N, Nøss PA, Gaarder C. Traumemanual: Oslo Universitetssykehus HF; 2011.
24. Prevention and Management of Postpartum Haemorrhage: Green-top Guideline No. 52. BJOG. 2017;124:e106-e49.
25. Pena-Rosas JP, De-Regil LM, Dowswell T, Viteri FE. Daily oral iron supplementation during pregnancy. Cochrane Database Syst Rev. 2012;12:CD004736.
26. Haider BA, Olofin I, Wang M, Spiegelman D, Ezzati M, Fawzi WW, et al. Anaemia, prenatal iron use, and risk of adverse pregnancy outcomes: systematic review and meta-analysis. BMJ. 2013;346:f3443.
27. Begley CM, Gyte GM, Devane D, McGuire W, Weeks A, Biesty LM. Active versus expectant management for women in the third stage of labour. Cochrane Database Syst Rev. 2019; 2:CD007412.
28. Westhoff G, Cotter AM, Tolosa JE. Prophylactic oxytocin for the third stage of labour to prevent postpartum haemorrhage. Cochrane Database Syst Rev. 2013; 10:CD001808.
29. Novikova N, Hofmeyr GJ, Cluver C. Tranexamic acid for preventing postpartum haemorrhage. Cochrane Database Syst Rev. 2015; 6:CD007872.
30. Simonazzi G, Bisulli M, Saccone G, Moro E, Marshall A, Berghella V. Tranexamic acid for preventing postpartum blood loss after cesarean delivery: a systematic review and meta-analysis of randomized controlled trials. Acta Obstet Gynecol Scand. 2016;95:28-37.
31. Hofmeyr GJ, Mshweshwe NT, Gulmezoglu AM. Controlled cord traction for the third stage of labour. Cochrane Database Syst Rev. 2015;1:CD008020.
32. Hutton EK, Hassan ES. Late vs early clamping of the umbilical cord in full-term neonates: systematic review and meta-analysis of controlled trials. JAMA. 2007;297(11):1241-52.
33. Hofmeyr GJ, Abdel-Aleem H, Abdel-Aleem MA. Uterine massage for preventing postpartum haemorrhage. Cochrane Database Syst Rev. 2013:CD006431.
34. Combs CA, Laros RK, Jr. Prolonged third stage of labor: morbidity and risk factors. Obstet Gynecol. 1991;77:863-7.
35. Weeks AD. The retained placenta. Best Prac Res Clin Obstet Gynaecol. 2008;22:1103-17.
36. Ford JB, Roberts CL, Bell JC, Algert CS, Morris JM. Postpartum haemorrhage occurrence and recurrence: a population-based study. Med J Austr. 2007;187:391-3.