- Det er stor risiko for kreft ved AIS.
- Cytologibasert screening er bedre til å detektere CIN enn AIS.
- HPV-basert screening finner flere AIS enn cytologiscreening.
- 20% av cervixcarcinom er adenocarcinomer.
- Adenocarcinomer i cervix deles inn i HPV- og ikke HPV-assosierte adenocarcinomer, hvorav sistnevnte utgjør ca. 15% av adenocarcinomene (1).
- HPV 16, 18 og 45 forårsaker 94% av adenocarcinomene (2).
Stor andel kreft
AIS i cervixcytologi forekommer svært sjeldent, med ca 130 tilfeller per år som utgjør 0,3‰ av alle celleprøver i Norge. Men, når cytologi angir AIS er det svært ofte behandlingstrengende sykdom. Upublisert rådata fra Kreftregisteret i perioden 2015-2018 viser totalt 521 kvinner med AIS i cervixcytologi. Så langt har man påvist hele 18% adenocarcinom, 1% plateepitelcarcinom, 2% cancer uteri, 2% ikke spesifisert cancer, 44% AIS og 17% CIN2-3, det vil si 85% behandlingstrengende forandringer i løpet av 5 års oppfølgingstid hos disse kvinnene (personlig meddelelse fra Gry B Skaare, Kreftregisteret 2021). Det er derfor viktig med rask avklaring og verifisering av diagnosen så pasienten får rett behandling. I andre europeiske land som England og Sverige utføres eksisjon (konisering) direkte utfra AIS i cytologi (uten å ta portiobiopsier og cervixutskrap på forhånd), etter at endometriekreft er utelukket hos de eldre [3] [4].
Utredning
Ved AIS er kolposkopi ikke egnet da vi ikke har oversikt over forandringene oppe i cervikalkanalen, samt at AIS oftest ikke har de samme typiske kolposkopiske forandringene som CIN (Bilde 1). For å utelukke livmorhalskreft tas biopsier og cervixutskrap med skarp curette. Histologi bør sendes prioritert, der det bes om svar innen 1 uke.
Hos kvinner over 40 år bør kreft i livmoren utelukkes.
Cervixutskrap har generelt lav diagnostisk verdi fordi stroma ikke kan vurderes, samt at det ofte er utilstrekkelig materiale (5, 6). Dersom biopsier og cervixutskrap besvares som normale, kan man ikke stole på at prøvetakingen har fanget opp sykdommen. Be derfor patologen se på cytologiprøven en gang til. Dersom AIS-diagnosen opprettholdes, bør man utføre eksisjon. Dersom AIS-diagnosen i cytologi endres til en mer benign tilstand der behandling kan avventes, anbefales kontroll om 2 måneder med cytologi og HPV. Dersom kontrollcytologi viser AIS på nytt, bør man utføre eksisjon.
Behandling
Ved AIS skal konisering prioriteres raskere enn CIN2 og CIN3 på grunn av høy risiko for at det kan foreligge kreft. Koniseringen av AIS er vanskelig, og siden det er såpass sjeldent, bør det være noen få erfarne kolposkopører som utfører dette inngrepet. I Sverige jobber man for at dette skal sentraliseres.
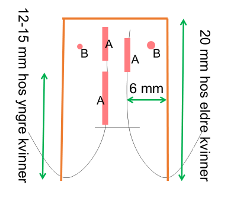
Figur 1. Figuren viser hvordan AIS skal behandles. Anlegg en sylinderformet, høy eksisjon for å få med «skip lesions» (A) som er til stede i ca 15%. Gå minst 6 mm lateralt og unngå sylinderformet slynge for å få med hele lengden på de endocervicale kryptene (B), da AIS kan gå helt ned i bunnen av disse kryptene (bilde fra A.Singer).
Bueformet slynge, nål eller laser?
Trekantslynge er ikke egnet for eksisjon da det er risiko for inadekvat fjerning av kryptene slik at sykt vev står igjen (Figur 1). Man bør etterstrebe ett preparat.
Hos kvinner med barneønske og transformasjonssone type 1 eller 2 bør en sylinderformet eksisjon med høyde 12-15 mm utføres. Bueformet slynge kan brukes. I tillegg bør eksisjonen være dyp nok lateralt for å sikre at man får med seg kryptene (minimum 6 mm dybde).
Hos kvinner som ikke lenger har barneønske, bør det utføres en sylinderformet høy eksisjon (20-25mm). I tillegg bør eksisjonen også her være 6 mm dyp til sidene for å sikre at kryptene er med. Diaterminål eller laser er best å bruke for å etterstrebe et preparat. Dersom bueformet slynge brukes, bør det i tillegg gjøres en «tophat», som er en mindre buet eksisjon av gjenværende cervikalkanal hvis man ikke har kommet høyt nok opp i kanalen. Husk å merke øvre reseksjonsrand. Etter eksisjon skal det gjøres cervikalt utskrap.
Oppfølging:
Dersom histologisvar angir ikke frie render, bør man i utgangspunktet utføre ny konisering. Dersom pasient har fremtidig barneønske, kan man vurdere kontroll innen 2-3 måneder med cytologi og HPV. Oppfølgingscytologi må være representativ, dvs inneholde både plate- og kjertelepitel. Ved persisterende HPV etter konisering bør hysterektomi diskuteres etter avsluttet barneønske. Ellers bør man vurdere rekonisering. Dersom det er frie render, men vanskelig å ta representative prøver fra stenotisk cervikalkanal til tross for blokking, bør hysterektomi anbefales, også ved negativ HPV test.
Referanser:
1. Kurman R CM, Herrington CS, Young RH: WHO classification of tumours of female reproductive organs. Lyon: IARC Publications; 2014.
2. de Sanjose S, Quint WG, Alemany L, Geraets DT, Klaustermeier JE, Lloveras B, Tous S, Felix A, Bravo LE, Shin HR et al: Human papillomavirus genotype attribution in invasive cervical cancer: a retrospective cross-sectional worldwide study. The Lancet Oncology 2010, 11(11):1048-1056.
3. Cervixcancerprevention. Nationelt vårdprogram, version 2.3 [https://nkcx.se/templates/nationellt-vardprogram-cervixcancerprevention.pdf]
4. NHS Cervical screening programme. Colposcopy and Programme Management [https://www.gov.uk/government/publications/cervical-screening-programme-and-colposcopy-management]
5. Mogensen ST, Bak M, Dueholm M, Frost L, Knoblauch NO, Praest J, Svanholm H: Cytobrush and endocervical curettage in the diagnosis of dysplasia and malignancy of the uterine cervix. Acta obstetricia et gynecologica Scandinavica 1997, 76(1):69-73.
6. Baasland I, Hagen B, Vogt C, Valla M, Romundstad PR: Colposcopy and additive diagnostic value of biopsies from colposcopy-negative areas to detect cervical dysplasia. Acta obstetricia et gynecologica Scandinavica 2016, 95(11):1258-1263.
