ICD-10 Koder
N 91.0 Primær amenoré
N 91.1 Sekundær amenoré
Anbefalinger
Vi foreslår
- Vi foreslår at alle pasienter med amenoré (primær og sekundær) henvises til gynekolog
- Vi foreslår i dette kapitlet en klassifisering av amenoré samt algoritme for evaluering vi mener er anvendelig i klinisk praksis.
Vi anbefaler
- Vi anbefaler regulering av under- og overvekt og råd om trening
- Vi anbefaler at pasienter med hyperprolaktinemi (WHO gruppe V og VI) behandles i samråd med endokrinolog og amenoreiske pasienter med normalt prolaktin nivå og påvist hypothalamisk / hypofysær tumor (WHO gruppe VII) henvises til nevrolog
- Flerregional behandlingstjeneste for usikker somatisk kjønnsutvikling bør konfereres for å vurdere tidspunkt for fjerning av XY gonader og sikre at pasienten er informert og kan samtykke
Viktig informasjon
Amenore er et symptom og ikke en diagnose. Tidligere historie, klinisk undersøkelse og utvalgt diagnostikk er tilstrekkelig for å finne årsaken og stille en diagnose i de fleste tilfellene.
Pasienter med sjeldne tilstander som usikker somatisk kjønnsutvikling (DSD/disorders of sex development) skal henvises til flerregional behandlingstjeneste ved Haukeland Universitetssykehus eller Oslo Universitetssykehus.
Litteratursøk
Pyramidesøk, Up to date, Pub-med, National Institute for Health and Clinical Exellence (NICE), Cochrane Database
Definisjon (1, 2)
Primær amenoré – manglende menstruasjon ved 16 års alder hos pasienter med normal utvikling av sekundære kjønnskarakteristika.
Forsinket pubertet - manglende menstruasjon ved 14 års alder hos pasienter uten utvikling av sekundære kjønnskarakteristika.
Sekunder amenoré – pasienter med tidligere regelmessig menstruasjon hvor det ikke har tilkommet vaginal blødning i løpet av de siste 3 måneder eller hos pasienter med tidligere uregelmessig menstruasjon hvor det ikke har tilkommet vaginal blødning siste 6 måneder.
Oligomenore – blødningsintervall > 35 dager over seks måneder eller mindre en 9 sykluser i løpet av 1 år.
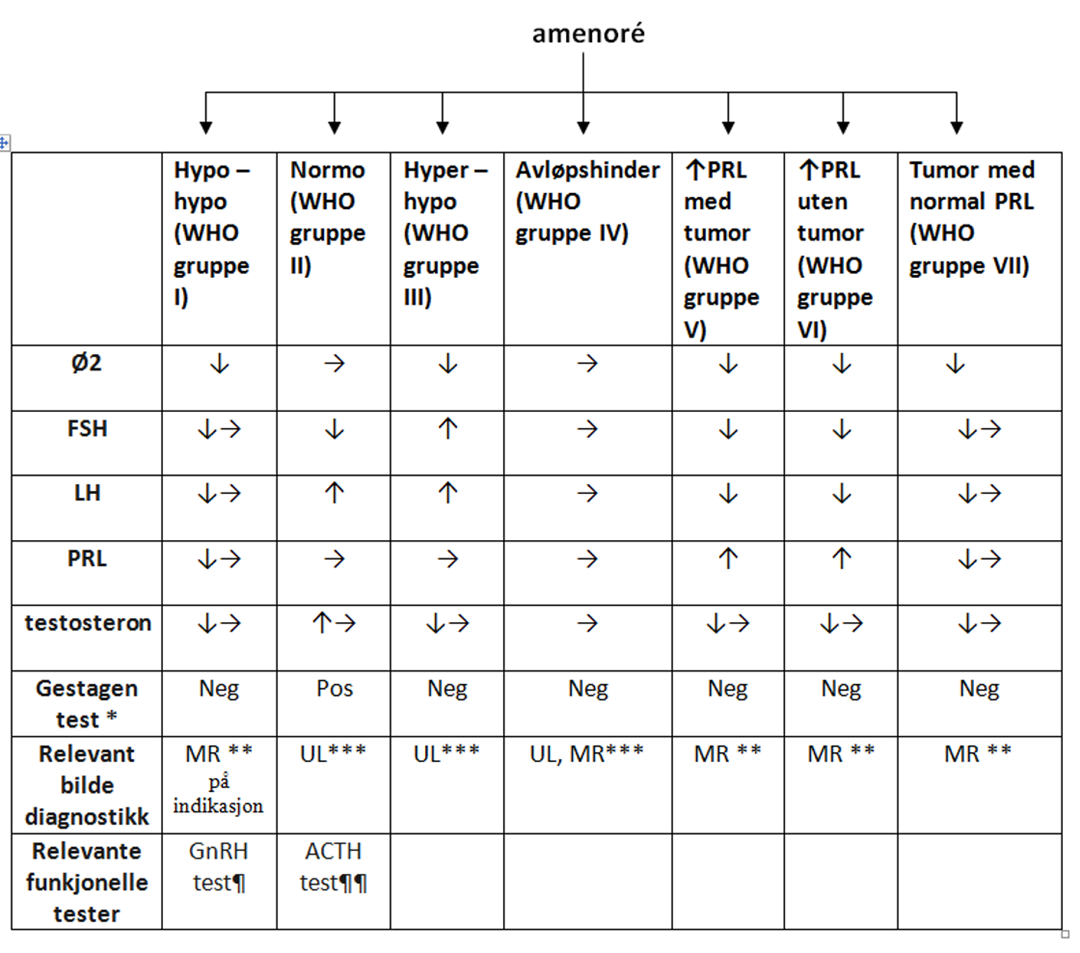
Klassifisering av amenoré

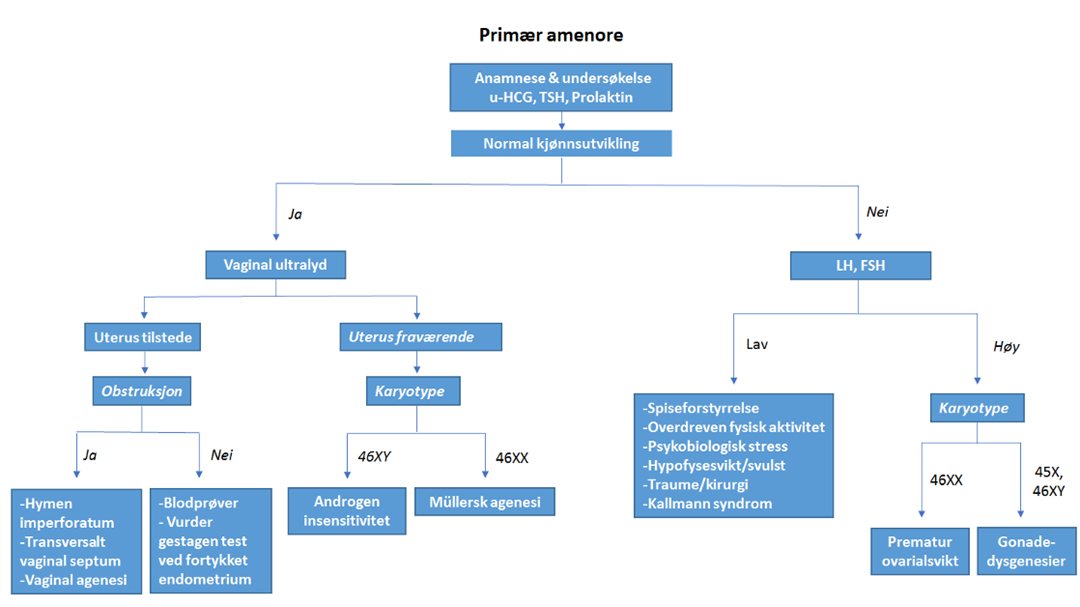
Algoritme for evaluering av primær amenore
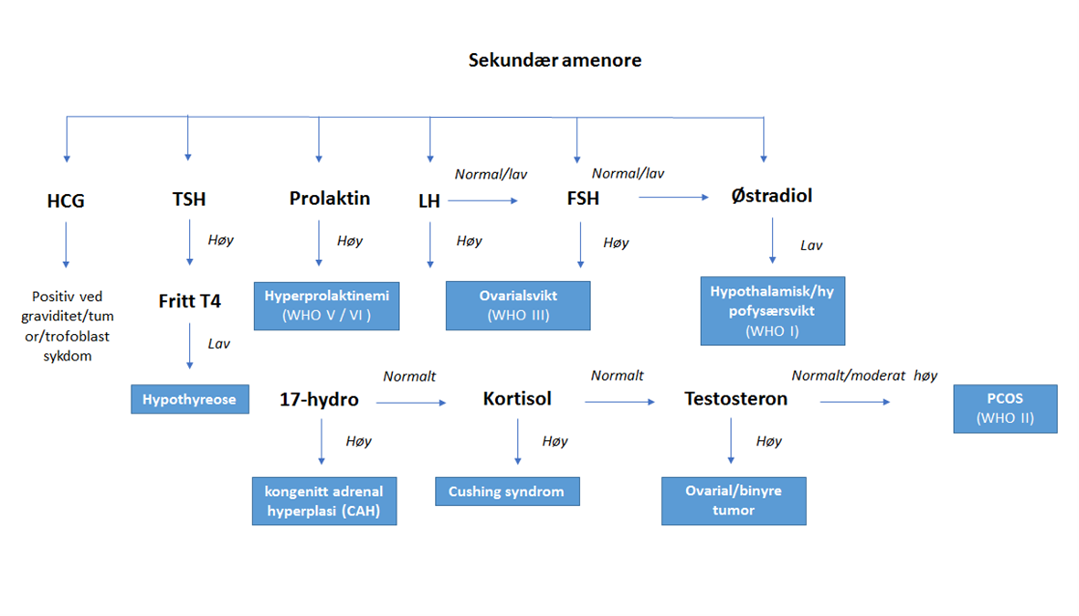
Algoritme for evaluering av sekundær amenore
Epidemiologi (2-5)
Forekomst
Amenoré oppstår hos 3-4 % hos kvinner i reproduktiv alder som ikke er gravide/ammer.
Etiologi
De fleste årsaker til primær og sekundær amenoré er like og enhver årsak til sekundær amenoré kan og være årsak til primær amenoré
-
WHO gruppe I - Hypothalamisk/hypofysær svikt - Hypogonadotrop hypogonadisme (1, 6-12)
Primær amenoré
- fysiologisk sen pubertetsutvikling (16 år)
- anoreksi og vekttap
- overdreven fysisk trening
- stress
- kronisk sykdom
- Kallmanns syndrom
- hypofysesvikt
- hypofysesvulster (prolaktinom, kraniofaryngeom, andre tumores)
- traume eller kirurgi
Sekundær amenoré
- Vekttap og spiseforstyrrelser (anorexia nervosa og bulimia nervosa)
- Eksessiv trening (maraton løpere, ballett dansere)
- Stress
- Iatrogen (intrakraniell kirurgi / bestråling / kjemoterapi)
- Sarkoidose
- Tuberkulose
- Sheehan syndrom (hypoperfusjonsskade av hypofysen ved uttalt blødning under fødsel)
- Idiopatisk
-
WHO gruppe II - Hypothalamisk/hypofysær dysfunksjon (1, 13-16)
- Polycystisk ovariesyndrom (PCOS) (se eget kapittel om PCO/PCOS)
- Ikke-PCOS relaterte årsaker til normogonadotrop anovulasjon – funksjonell hypothalamisk amenoré
- Vekttap og spiseforstyrrelser (anorexia nervosa og bulimia nervosa)
- Eksessiv trening (maraton løpere, ballett dansere)
- Kroniske sykdommer (diabetes mellitus, nyre-, lever- og lungesykdommer, morbus Addison)
- Leptinmangel
-
WHO gruppe III - hypergonadotrop hypogonadisme (1, 17-28)
Primær amenoré
- Turners syndrom og varianter (45,X0 karyotype), 1 per 2000-5000, men også andre tilstander med gonadesvikt som Swyer syndrom (46XY karyotype) (se eget kapittel om genitale misdannelser)
- Enzymmangel som hindrer normal østrogenproduksjon, forårsaket av mutasjon i CYP17-genet (17α-hydroksylasemangel, 17,20-desmolasemangel)
- gonadotropinreseptormutasjon (LH-reseptormutasjon, FSH-reseptormutasjon)
- Ovarial dysgenesi/agenesi (eks Turners syndrom) (se eget kapittel om genitale misdannelser)
- Iatrogen (bestråling eller kjemoterapi)
- Primær ovarial insuffisiens (se eget kapittel om POI)
Sekundær amenoré
- Primær ovarial insuffisiens (se eget kapittel om POI)
- Gonadotropinresistente ovarier (Savage syndrom)
- Galactosemia
- Iatrogen (bestråling, kjemoterapi, kirurgi)
- Gonadedysgenesi
-
WHO gruppe IV - normogonadotrop - medfødte eller ervevede uterovaginale avvik (1, 29-34)
Primær amenoré (se også kapittelet om genitale misdannelser)
- Hymen imperforatum, forekomst 1-2 % av de med primær amenoré
- Medfødte misdannelser i uterus og vagina (f.eks fraværende endometrium, sjelden)
- Müllersk agenesi (agenesi av uterus og vagina) (Mayer-Rokitansky-Küster-Hauser syndrom) forekomst 1 per 4000-10 000
- Transversalt vaginalt septum (1 per 80 000)
- Androgen insensitivitet syndrom (AIS), forekomst 1 per 10 000, høy testosteron og karyotype 46 XY
Sekundær amenoré
- Ashermanns syndrom
- sekundært etter uterinkirurgi; revisio, spesielt postpartum
- sekundært til infeksjoner; Pelvic Inflammatory Disease (PID), Intra Uterine Devise (IUD) relatert, tuberkulose, schistosomiasis
- Endometrieablasjon
-
WHO gruppe V - Hyperprolaktinemi med hypofysetumor (1, 2)
- prolaktinom
-
WHO gruppe VI - Hyperprolaktinemi uten hypofysetumor (1, 2)
- Medikamenter (metoklopramid, antipsykotika)
- Hypothyreose
- Uremi
- Sykdommer i hypothalamus
- Idiopatisk
-
WHO gruppe VII - Hypothalamisk/hypofysær tumor uten hyperprolaktinemi (12)
- Kraniofaryngeom, germinom, sarcoid/tuberkuløst granulom, dermoidcyster, adenomer
- Andre årsaker
- Thyreoideaforstyrrelser
- Binyreforstyrrelser /Cushing syndrom
- Gonadotropin resistens
- Graviditet
Risikofaktorer for utvikling av amenore
- Genetikk (familiær sen menarke)
- Spiseforstyrrelser
- Stor fysisk aktivitet
- Stress
- Kronisk sykdom
- Sult
- Store postpartumblødninger – Sheehans syndrom
- Revisio, spesielt postpartum revisio kan gi Ashermann syndrom
Diagnostikk (1, 2, 35, 36)
Evaluering av amenoré (sekundær) starter oftest med HCG test for å utelukke svangerskap. Man bør også utelukke thyroidea- og binyreforstyrrelser.
Primær amenoré
1. Anamnese
- Pubertetsutvikling i familien
- Tidligere vekst
- Tidligere sykdommer
- Fysisk aktivitet
- Spisevaner
- Psykologisk og følelsesmessig stress
- Hodepine/synsfelt
2. Klinisk undersøkelse
- De fleste medfødte anomalier kan diagnostiseres ved klinisk undersøkelse
- Vurdering av sekundære kjønnskarakteristika (Tanners inndeling): kjønnsbehåring (aksiller og pubes), brystutvikling
- Høyde og vekt
- Dysmorfe trekk, Turner stigmata, virilisering
- Gynekologisk undersøkelse gjøres kun når sekundære kjønnskarakteristika er til stede
- Ikke nødvendig ved forsinket pubertet
- Sondering av vagina med vattpinne
- Evt. avtales til neste konsultasjon slik at pasienten er forberedt
- Evt. rektal eksplorasjon
- Luktesans (Kallmanns syndrom)
3. Biokjemiske/laboratoriske undersøkelser
- Rutine undersøkelser: Østradiol, FSH, LH, Prolaktin, TSH, FT4, evt u-hCG
- Behovsprøvede undersøkelser: testosteron, SHBG, androstendion, 17-OH-progesteron, 11-deoxycortisol, anti-TPO, anti-21 hydroxylase, karyotype
4. Bildediagnostikk
- Ultralyd (vaginal, perineal, rektal eller abdominal) eller MR abdomen/bekken
- MR hypofyse
- Vurdere røntgenundersøkelse av hånd (for vurdering av skjelettalder, menarke forventes normalt ved skjelettalder på 13-14 år), Rtg. columna (skjelettmalformasjoner), Rtg. urografi (nyre-abnormaliteter), DEXA-scan (Dual energy X- ray absorptiometry scan) for vurdering av bentetthet
5. Andre undersøkelser
- Synsfeltundersøkelse (store hypofyse tumores)
Sekundær amenoré
1. Klinisk undersøkelse med helst vaginal ultralyd
- Høyde og vekt (BMI)
- Fettfordeling (sentralt mot perifert kroppsfett)
- Akne og hirsutisme (hyperandrogenisme)
- Acanthosis nigricans, pigmentering av huden (diabetes og insulinresistens)
- Galaktore (hyperprolaktinemi)
- Struma (thyroidea sykdom)
- Vurdering av endometrium ved ultralyd (tykkelse av normalt endometrium er direkte relatert til østrogen nivå i serum)
2. Biokjemiske/laboratoriske undersøkelser
- Basale laboratorieprøver: s-hCG/u-hCG, TSH, Prolaktin, FSH, østradiol
- Ved androgenisering: testosterone, androstendion, SHBG, 17-OH-progesteron, 11-deoxycortisol, ACTH-test, test på insulinresistens (glukosebelastning m/insulin)
- Ved ovarial insuffisiens (se eget kapittel om POI)
3. Andre undersøkelser
For å teste anatomiske forutsetninger for menstrusjonsblødning:
- Gestagentest (medroxyprogesteronacetat 5-10 mg i 10 dager)
- Østrogen/gestagentest (f.eks østradiol 2 mg/d i 21 dager, deretter -gestagen 10 mg /d i 7-10 dager)
- Hysteroskopi for å oppdage endometriumdestrusjoner og Ashermans syndrom
- MR hypofyse
- Synsfeltundersøkelse
Differensialdiagnoser
- Graviditet
- Amming
- Menopause
- Hypothyreose
Behandling (1, 2, 8, 9, 17, 29, 37)
Primær amenoré
- Jenter med begynnende pubertetsutvikling (forsinket pubertet)
- Berolige
- Avvente
- Gestagen bortfallstest
- Hypoøstrogene tilstander
- Østrogen/gestagen substitusjonsbehandling (Hormone Replacement Therapy (HRT))
- Vurdere p-pille kontinuerlig (hypogonadotrop hypogonadisme), ikke førstevalg
- Rent østrogen tilstrekkelig ved fravær av uterus
- Hyperprolaktinemi med eller uten tumor behandles av endokrinolog
- Dopaminagonister: cabergolin (Dostinex) eller Quinagolid (Norprolac)
- Turner syndrom (se eget kapittel om genitale misdannelser)
- Eggdonasjon
- Fjerning av XY-gonader pga. risiko for malign utvikling
- Drenasjeoperasjoner ved misdannelser med hematometra eller hematokolpos
- Ved Mayer-Rokitansky-Küster-Hauser syndrom må andre utviklingsavvik utelukkes (skjelettmisdannelser, urinveispatologi), se eget kapittel om genitale misdannelser
Sekundær amenoré
- Barneønske
- WHO I: daglige injeksjoner av HMG (humant menopausalt gonadotropin) eller pulsatil GnRH-infusjon. Vurdere assistert befruktning med HMG stimulering.
- WHO II: (se eget kapittel om PCO/PCOS)
- WHO III: HRT, kortikosteroider, eggdonasjon
- WHO IV: som oftest ikke mulig, kirurgi i noen tilfelle (Asherman)
- WHO V og VI: cabergolin (Dostinex) eller Quinagolid (Norprolac)
- WHO VII: FSH- eller HMG-injeksjoner
- Ikke barneønske
- HRT ved alle hypoøstrogene tilstander
- Behovet for induksjon av regelmessige avbrudsblødninger ved amenoré/ oligomenore og endogen østrogenproduksjon vurderes (se eget kapittel om PCO/PCOS)
- Cabergolin (Dostinex) eller Quinagolid (Norprolac) ved hyperprolaktinemi med eller uten tumor
- Kognitiv terapi
Oppfølging
Individuell i forhold til behandlingsregime
Komplikasjoner og konsekvenser for senere helse
- Fravær av menstruasjon i seg selv har ingen skadelig effekt på helsen, men amenore kan representere en underliggende lidelse som krever behandling (f. eks hypofysetumor, hypoøstrogenisme, infertilitet)
- Sen pubertetsutvikling kan hemme en normal psykoseksuell utvikling
- Hypoøstrogene tilstander kan medføre redusert velvære og psykisk helse, osteoporose, på lang sikt økt risiko for hjerte-kar sykdom og høyere dødelighet
- dysgerminomutvikling i 46XY-gonader
- Turner syndrom har økt risiko for øreproblemer, autoimmune sykdommer, forhøyede leverenzymer, diabetes/metabolsk syndrom, hjertefeil og aortaneurisme, cøliaki og inflamatorisk tarmsykdom (se eget kapittel om genitale misdannelser for oppfølgingsalgoritme)
Prognose
- Generelt god, men økt sykelighet og dødelighet ved hypoøstrogene tilstander
- Fertilitet, som regel kun mulig ved hypothalamisk/hypofysær svikt og ved mindre vaginale fusjonsdefekter. Eggdonasjon i prinsippet mulig for alle som har uterus med funksjonelt endometrium
Referanser
1. Hugh S. Taylor LP, Emre Seli. Speroff`s Clinical Gynecologic Endocrinology and Infertility. 2020, 9th edition.
2. Current evaluation of amenorrhea. Fertil Steril. 2008;90(5 Suppl):S219-S25.
3. Golden NH, Carlson JL. The pathophysiology of amenorrhea in the adolescent. Ann N Y Acad Sci. 2008;1135:163-78.
4. Hoffman B, Bradshaw KD. Delayed puberty and amenorrhea. Semin Reprod Med. 2003;21(4):353-62.
5. Baird DT. Amenorrhoea. The Lancet. 1997;350(9073):275-9.
6. Forni PE, Wray S. GnRH, anosmia and hypogonadotropic hypogonadism - Where are we? Front Neuroendocrinol. 2014.
7. Seminara SB, Hayes FJ, Crowley WF, Jr. Gonadotropin-releasing hormone deficiency in the human (idiopathic hypogonadotropic hypogonadism and Kallmann's syndrome): pathophysiological and genetic considerations. Endocr Rev. 1998;19(5):521-39.
8. Patel SS, Bamigboye V. Hyperprolactinaemia. J Obstet Gynaecol. 2007;27(5):455-9.
9. Pickett CA. Diagnosis and management of pituitary tumors: recent advances. Prim Care. 2003;30(4):765-89.
10. Till K. Craniopharyngioma. Childs Brain. 1982;9(3-4):179-87.
11. Lichter AS, Wara WM, Sheline GE, Townsend JJ, Wilson CB. The treatment of craniopharyngiomas. Int J Radiat Oncol Biol Phys. 1977;2(7-8):675-83.
12. Palmer J.D. SA, Shi W. . Craniopharyngioma. In: Chang E., Brown P., Lo S., Sahgal A., Suh J. (eds). Adult CNS Radiation Oncology Springer, Cham https://doiorg/101007/978-3-319-42878-9_3. 2018.
13. Lauritsen MP, Pinborg A, Loft A, Petersen JH, Mikkelsen AL, Bjerge MR, et al. Revised criteria for PCOS in WHO Group II anovulatory infertility - a revival of hypothalamic amenorrhoea? Clin Endocrinol (Oxf). 2014.
14. Warren MP, Voussoughian F, Geer EB, Hyle EP, Adberg CL, Ramos RH. Functional hypothalamic amenorrhea: hypoleptinemia and disordered eating. J Clin Endocrinol Metab. 1999;84(3):873-7.
15. Miller KK, Grinspoon S, Gleysteen S, Grieco KA, Ciampa J, Breu J, et al. Preservation of neuroendocrine control of reproductive function despite severe undernutrition. J Clin Endocrinol Metab. 2004;89(9):4434-8.
16. Gaete X, Vivanco M, Eyzaguirre FC, Lopez P, Rhumie HK, Unanue N, et al. Menstrual cycle irregularities and their relationship with HbA1c and insulin dose in adolescents with type 1 diabetes mellitus. FertilSteril. 2010;94(5):1822-6.
17. Classic pages in obstetrics and gynecology by Henry H. Turner. A syndrome of infantilism, congenital webbed neck, and cubitus valgus. Endocrinology, vol. 23, pp. 566-574, 1938. Am J Obstet Gynecol. 1972;113(2):279.
18. Hawkins JR. Mutational analysis of SRY in XY females. Hum Mutat. 1993;2(5):347-50.
19. Timmreck LS, Reindollar RH. Contemporary issues in primary amenorrhea. Obstet Gynecol Clin North Am. 2003;30(2):287-302.
20. Goldsmith O, Solomon DH, Horton R. Hypogonadism and mineralocorticoid excess. The 17-hydroxylase deficiency syndrome. N Engl J Med. 1967;277(13):673-7.
21. Beranova M, Oliveira LM, Bedecarrats GY, Schipani E, Vallejo M, Ammini AC, et al. Prevalence, phenotypic spectrum, and modes of inheritance of gonadotropin-releasing hormone receptor mutations in idiopathic hypogonadotropic hypogonadism. J Clin Endocrinol Metab. 2001;86(4):1580-8.
22. Ahmed SR, Shalet SM, Campbell RH, Deakin DP. Primary gonadal damage following treatment of brain tumors in childhood. J Pediatr. 1983;103(4):562-5.
23. Kim MH. "Gonadotropin-resistant ovaries" syndrome in association with secondary amenorrhea. Am J Obstet Gynecol. 1974;120(2):257-63.
24. Tapanainen JS, Vaskivuo T, Aittomaki K, Huhtaniemi IT. Inactivating FSH receptor mutations and gonadal dysfunction. Mol Cell Endocrinol. 1998;145(1-2):129-35.
25. Stillman RJ, Schinfeld JS, Schiff I, Gelber RD, Greenberger J, Larson M, et al. Ovarian failure in long-term survivors of childhood malignancy. Am J Obstet Gynecol. 1981;139(1):62-6.
26. Morrison JC, Givens JR, Wiser WL, Fish SA. Mumps oophoritis: a cause of premature menopause. Fertil Steril. 1975;26(7):655-9.
27. Alper MM, Garner PR, Seibel MM. Premature ovarian failure. Current concepts. J Reprod Med. 1986;31(8):699-708.
28. Nishi Y, Hamamoto K, Kajiyama M, Kawamura I. The Perrault syndrome: clinical report and review. Am J Med Genet. 1988;31(3):623-9.
29. Breech LL, Laufer MR. Mullerian anomalies. Obstet Gynecol Clin North Am. 2009;36(1):47-68.
30. Buttram VC, Jr., Gibbons WE. Mullerian anomalies: a proposed classification. (An analysis of 144 cases). Fertil Steril. 1979;32(1):40-6.
31. Cramer DW, Goldstein DP, Fraer C, Reichardt JK. Vaginal agenesis (Mayer-Rokitansky-Kuster-Hauser syndrome) associated with the N314D mutation of galactose-1-phosphate uridyl transferase (GALT). Mol Hum Reprod. 1996;2(3):145-8.
32. Morcel K, Camborieux L, Guerrier D. Mayer-Rokitansky-Kuster-Hauser (MRKH) syndrome. Orphanet J Rare Dis. 2007;2:13.
33. Amrhein JA, Meyer WJ, III, Jones HW, Jr., Migeon CJ. Androgen insensitivity in man: evidence for genetic heterogeneity. Proc Natl Acad Sci U S A. 1976;73(3):891-4.
34. Klein SM, Garcia CR. Asherman's syndrome: a critique and current review. Fertil Steril. 1973;24(9):722-35.
35. Klein DA, Poth MA. Amenorrhea: an approach to diagnosis and management. Am Fam Physician. 2013;87(11):781-8.
36. Krassas GE. Thyroid disease and female reproduction. Fertil Steril. 2000;74(6):1063-70.
37. Manuel M, Katayama PK, Jones HW, Jr. The age of occurrence of gonadal tumors in intersex patients with a Y chromosome. Am J Obstet Gynecol. 1976;124(3):293-300.